题目内容
可逆反应N2(g)+3H2(g)?2NH3(g),△H=-Q KJ/mol(Q>0).有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molN2和3molH2,在一定条件下达到平衡时放出热量为Q1KJ;在相同条件下,向乙容器中加入2molNH3达到平衡后吸收热量为Q2KJ,已知Q1=4Q2.下列叙述不正确的是( )
| A、达到平衡时,两容器中反应物的转化率不同 |
| B、达到平衡时,甲中NH3的体积分数与乙相等 |
| C、达到平衡后,再向乙中加入0.2moLN2、0.6molH2、1.6molNH3,平衡向生成NH3的方向移动 |
| D、乙中的热化学反应方程式为2NH3(g)?N2(g)+3H2(g);△H=+Q2KJ/mol |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、由于1molN2和3molH2完全反应可以生成2molNH3,所以甲乙两个体系的平衡状态是一样的,即对应气体的浓度完全相同. 对于同一可逆反应,相同条件下,正反应的反应热与逆反应的反应热,数值相等,符号相反,N2和H2完全反应时放热Q,则NH3完全分解时吸热也是Q,
根据三段式利用x表示出平衡时甲容器内反应混合物各组分的物质的量为 N2(1-x )mol、H2(3-3x )mol、NH32xmol,放出热量Q1=xQkJ;
则乙容器反应混合物各组分的物质的量也是为 N2(1-x )mol、H2(3-3x )mol、NH32xmol,所以分解的NH3的物质的量为(2-2x)mol,吸收热量(1-x)QkJ,利用Q1=3Q2,列放出求出x的值,转化的N2为x,利用转化率定义计算.
B、达到的平衡是相同平衡;
C、依据平衡常数和浓度商比较判断;
D、反应热是全部反应时放出的热量.
根据三段式利用x表示出平衡时甲容器内反应混合物各组分的物质的量为 N2(1-x )mol、H2(3-3x )mol、NH32xmol,放出热量Q1=xQkJ;
则乙容器反应混合物各组分的物质的量也是为 N2(1-x )mol、H2(3-3x )mol、NH32xmol,所以分解的NH3的物质的量为(2-2x)mol,吸收热量(1-x)QkJ,利用Q1=3Q2,列放出求出x的值,转化的N2为x,利用转化率定义计算.
B、达到的平衡是相同平衡;
C、依据平衡常数和浓度商比较判断;
D、反应热是全部反应时放出的热量.
解答:
解:A、由于1molN2和3molH2完全反应可以生成2molNH3,所以甲乙两个体系的平衡状态是一样的,即三种气体的浓度完全相同,对于同一可逆反应,相同条件下,正反应的反应热与逆反应的反应热,数值相等,符号相反.N2和H2完全反应时放热Q,则NH3完全分解时吸热也是Q,
假设甲容器中的参加反应的氮气的物质的量为xmol,所以:
对于甲容器:N2(g)+3H2(g)?2NH3(g)△H=-QkJ/mol
起始(mol):1 3 0
变化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
所以Q1=xQkJ,
乙容器反应混合物各组分的物质的量也是为N2(1-x )mol、H2(3-3x )mol、NH32xmol,所以分解的NH3的物质的量为(2-2x)mol,
对于乙容器:2NH3(g)?N2(g)+3H2(g)△H=+QkJ/mol,故吸收的热量Q2=
×QkJ=(1-x)QkJ,
所以4(1-x)Q=xQ,解得x=0.8,所以N2的转化率为
×100%=80%,NH3的转化率为
=20%,故A正确;
B、甲乙容器中达到的平衡是相同平衡,所以氨气的体积分数相同,故B正确;
C、依据A分析计算得到平衡物质的量N2为0.2mol,H2为0.6mol,NH3为1.6mol,再向乙中加入0.2mol N2(g)、0.6mol H2(g)和1.6mol NH3(g),相当于增大压强,平衡正向进行,故C正确;
D、反应是可逆反应,乙中反应的热化学方程式为2NH3(g)?N2(g)+3H2(g)△H>+Q2kJ/mol,故D错误;
故选D.
假设甲容器中的参加反应的氮气的物质的量为xmol,所以:
对于甲容器:N2(g)+3H2(g)?2NH3(g)△H=-QkJ/mol
起始(mol):1 3 0
变化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
所以Q1=xQkJ,
乙容器反应混合物各组分的物质的量也是为N2(1-x )mol、H2(3-3x )mol、NH32xmol,所以分解的NH3的物质的量为(2-2x)mol,
对于乙容器:2NH3(g)?N2(g)+3H2(g)△H=+QkJ/mol,故吸收的热量Q2=
| 2-2x |
| 2 |
所以4(1-x)Q=xQ,解得x=0.8,所以N2的转化率为
| 0.8 |
| 1 |
| 2-2x |
| 2 |
B、甲乙容器中达到的平衡是相同平衡,所以氨气的体积分数相同,故B正确;
C、依据A分析计算得到平衡物质的量N2为0.2mol,H2为0.6mol,NH3为1.6mol,再向乙中加入0.2mol N2(g)、0.6mol H2(g)和1.6mol NH3(g),相当于增大压强,平衡正向进行,故C正确;
D、反应是可逆反应,乙中反应的热化学方程式为2NH3(g)?N2(g)+3H2(g)△H>+Q2kJ/mol,故D错误;
故选D.
点评:本题考查化学平衡的分析判断,平衡状态特征的分析应用,等效平衡的判断转化率计算是解题关键,题目难度较大.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
下列各组物质中,满足表中图示物质在通常条件下一步转化关系的组合只有( )
| 序号 | X | Y | Z | W | 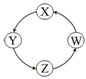 |
| ① | Cu | CuSO4 | Cu(OH)2 | CuO | |
| ② | Na | NaOH | Na2CO3 | NaCl | |
| ③ | Cl2 | Ca(ClO)2 | HClO | HCl | |
| ④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
| A、①②③ | B、①③④ |
| C、②③ | D、①④ |
一定温度下,向aL密闭容器中加入2molNO2(g),发生如下反应:2NO2?2NO+O2,此反应达到平衡状态时的标志是( )
| A、混合气体的颜色变浅 |
| B、混合气体的物质的量相等 |
| C、混合气中NO2、NO、O2物质的量之比为2:2:1 |
| D、单位时间内生成2nmolNO同时生成2nmolNO2 |
下列反应的离子方程式中,正确的是( )
| A、稀硫酸滴在银片上:2Ag+2H+=2Ag++H2↑ |
| B、稀硫酸与氢氧化钡溶液混合:SO42-+Ba2+=BaSO4↓ |
| C、盐酸滴在石灰石上:CaCO3+2H+=Ca2++CO2↑+H2O |
| D、把金属钠放入水中:Na+2H2O=Na++2OH-+H2↑ |
下列有关离子方程式与所述事实相符且正确的是( )
A、用惰性电极电解MgCl2溶液:2Cl-+2H2O
| ||||
| B、向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO42-=BaSO4↓+H2O | ||||
| C、(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2 | ||||
| D、C12通入澄清石灰水中:C12+2OH-=C1-+CIO-+H2O |
 A、B、C、D四种短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族.已知D原子最外层电子数是电子层数的3倍,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质.
A、B、C、D四种短周期元素,A、B、C同周期,A的原子半径是同周期中最大的;B、D同主族.已知D原子最外层电子数是电子层数的3倍,C元素的单质可以从A、B两元素组成的化合物的水溶液中置换出B元素的单质.