��Ŀ����
11���Ȼ���ͭ����Ҫ��ͭ��ϵ�л�����Ʒ���㷺Ӧ����ʯ�ͻ�������֯ӡȾ�����ϡ�ҽҩ����ơ��л��ϳɵ���ҵ��CuCl�����ڴ���ˮ��������������Ũ�Ƚϴ����ϵ���ڳ�ʪ��������ˮ���������Թ�ҵ����ͭΪԭ�ϣ���������������ֽ⼼����������ͭ���������Ȼ���ͭ������ͭ����Ҫ�ɷ���CuO��Cu��������������ͼ��ͼ1��
˼�����ش��������⣮
��1������ԭ�����ܽ�ʱ���ɵĻ�ԭ������������Һ���ȶ����ڣ���д����ʱ�����ӷ���ʽ��4Cu+10H++NO3-=4Cu2++NH4++3H2O���ܽ��¶�Ӧ������60��70�棬ԭ��������������ֽ⣮
��2����ԭ�Ȼ����õ�����Ʒ�Ļ�ѧʽΪ��NH4��2SO4��
��3��������Σ�����Һ��ø���Ʒ�IJ��裺������Ũ������ȴ�ᾧ�۹��ˢ�ϴ�� �ݸ��
��4����Ʒ��ϴ�ӷ����ǣ�����pH=2����ϴ��ˮϴ��������ϴʹ�õ���ϡ�����ᣮ����95%�ľƾ�ϴ���ƾ�ϴ��Ŀ���Ǿƾ��ӷ������ٵõ�����CuCl��Ʒ����ֹ��������
��5������������
��ȡ2.000g CuCl��Ʒ�����ʲ����뷴Ӧ��������һ������0.5000mol•L-1FeCl3��Һ�У���ˮϡ����200mL�õ���Һ��ȡ20.00mL ��0.1000mol•L-1��Ce��SO4��2��Һ�ζ����յ㣬����20.00mLCe��SO4��2��
�ٴ�ʵ���漰��Һ�����붨���ζ��Ļ��������У���������ͼ2�е�BC��
���йط�Ӧʽ��Fe3++CuCl�TFe2++Cu2++Cl- Ce4++Fe2+�TFe3++Ce3+
����Ʒ��CuCl����������99.50%��
���� ����ͭ���������������ܽ�õ���Һ��Ҫ������ͭ������淋ȣ�����������炙�ԭ����ͭ�����Ȼ���Ȼ�������Ӧ2CuSO4+��NH4��2SO3+2NH4Cl+H2O=2CuCl��+2��NH4��2SO4+H2SO4�����˵õ�����ΪCuCl����Һ��Ҫ������狀����
��1���ܽ�ʱ���ɵĻ�ԭ������������Һ���ȶ����ڣ�ͭ������狀�������Һ�б�������������ͭ���ӣ���������ӱ���ԭΪ笠����ӣ��¶ȹ�������炙�ֽ⣻
��2������������֪��Һ��Ҫ������狀����ᣬ�õ�����ƷΪ����泥�
��3�����������Һ�л������茶��壬���Ծ�������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����Ȳ��裻
��4���õ���CuCl��������ϴ��ˮϴ�������Ҵ�ϴ�ӣ��ƾ��ӷ����þƾ�ϴ��CuCl��Ʒ���ɿ��ٳ�ȥ��������ˮ�֣���ֹˮ�⡢����������ϡH2SO4ϴʱ�Ƿ���ϴ�ɾ�����ȡ���һ��ϴ��Һ�����Ƿ�������泥�����笠��Ĵ������ʵ����飻
��5����Һ����ʱ��������ƿ��ת����Һʱ����Һ����մ������ƿ�̶������棬�ڴ���ʽ�ζ��ܻ���ʱ��Ҫ�ѻ����������ĵ�λ�ã���ָ����һ�����������������ʽ�ɵõ�Ce4+��Fe2+��CuCl��n��Ce4+��=0.1000mol•L-1��0.02L=0.002mol����2.000g��Ʒ�к���n��CuCl��=10��0.002mol=0.02mol�����������������������ʽ���㣮
��� �⣺����ͭ���������������ܽ�õ���Һ��Ҫ������ͭ������淋ȣ�����������炙�ԭ����ͭ�����Ȼ���Ȼ�������Ӧ2CuSO4+��NH4��2SO3+2NH4Cl+H2O=2CuCl��+2��NH4��2SO4+H2SO4�����˵õ�����ΪCuCl����Һ��Ҫ������狀����
��1��ͭ������狀�������Һ�б�������������ͭ���ӣ����ᱵ��ԭΪ笠����ӣ���ʱ��������ԭ��Ӧ���ӷ���Ϊ4Cu+10H++NO3-=4Cu2++NH4++3H2O��
�ʴ�Ϊ��4Cu+10H++NO3-=4Cu2++NH4++3H2O������������ֽ⣻
��2������������֪��Һ��Ҫ������狀����ᣬ�õ�����ƷΪ����泥��ʴ�Ϊ����NH4��2SO4��
��3�����������Һ�л������茶��壬���Ծ�������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����Ȳ��裬�ʴ�Ϊ�����ˣ�
��4�������̿�֪������ϴ��ˮϴ��õ�����泥���Ӧ�������ᣬΪ��ֹCuCl�ܽ⣬���ܼ���������������ᣬҲ���ܼ������ᣬ��ֹ���������ʣ���Ʒ��ϴ�ӷ���������pH=2��ϡH2SO4ϴ������95%�ľƾ�ϴ�����Ҵ��е�ͣ��ӷ��������Ҵ�ϴ�ӣ��ɿ��ٳ�ȥ��������ˮ�֣���ֹˮ�⡢������
�ʴ�Ϊ��ϡ����ƾ��ӷ������ٵõ�����CuCl��Ʒ����ֹ��������
��5������Һ����ʱ��������ƿ��ת����Һʱ����Һ����մ������ƿ�̶������棬�ڴ���ʽ�ζ��ܻ���ʱ��Ҫ�ѻ����������ĵ�λ�ã���ָ����һ�������
��ѡBC��
�ʴ�Ϊ��BC��
��Fe3++CuCl=Fe2++Cu2++Cl-��Ce4++Fe2+=Fe3++Ce3+�ɵõ�Ce4+��Fe2+��CuCl��n��Ce4+��=0.1000mol•L-1��0.02L=0.002mol����2.000g��Ʒ�к���n��CuCl��=10��0.002mol=0.02mol������m��CuCl��=0.02mol��99.5g/mol=1.99g�������Ʒ��CuCl����������=$\frac{1.99g}{2.000g}$��100%=99.50%��
�ʴ�Ϊ��99.50%��
���� ���⿼����ͭ���仯�������ʵ�����Ӧ�ã���Ҫ���������ʺͷ�Ӧ������жϣ����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д� A��B��C�ֱ������ֳ����Ľ�����ǽ����ĵ��ʣ�D��E��F���dz������������������������ʾ��ת����ϵ������˵���д�����ǣ�������
A��B��C�ֱ������ֳ����Ľ�����ǽ����ĵ��ʣ�D��E��F���dz������������������������ʾ��ת����ϵ������˵���д�����ǣ�������| A�� | D��E��һ��������AԪ�� | B�� | ����B�϶��������� | ||
| C�� | A��B��C��һ����һ����O2 | D�� | ��A�Ƿǽ�������Bһ��Ϊ���� |
| A�� | ������������ѹ������о���� | |
| B�� | ˮ�ࡢ������ˮ�����ﶼ�ǹ�������Ʒ | |
| C�� | �������������������ά | |
| D�� | ʯӢ���������������ѧ���� |
| A�� | �����ʵ���Ũ�ȵ�������Һ����H2CO3 ��Na2CO3 ��NaHCO3 �ܣ�NH4��2CO3����c��CO32-���Ĵ�С��ϵΪ���ڣ��ܣ��ۣ��� | |
| B�� | pH=2��H2C2O4��Һ��pH=12��NaOH��Һ�������ϣ�c��Na+��+c��H+��=c��OH-��+c�� HC2O4-��+c�� C2O42-�� | |
| C�� | ��0.2 mol•L-1NaHCO3��Һ�м�������0.1 mol•L-1NaOH��Һ��c��CO32-����c��HCO3-����c��OH-����c��H+�� | |
| D�� | �����£�ͬŨ�ȵ�CH3COONa��CH3COOH��Һ�������ϣ���Һ��pH��7��c��CH3COOH��+c��OH-����c��Na+��+c��H+�� |
| A�� | ij��ɫ���廯��������ˮ�������õ���ɫ��Һ�е��뼸�η�̪�Լ�����Һ�ʺ�ɫ��֤�����ְ�ɫ���廯����һ���Ǽ� | |
| B�� | ��ij��ɫ��Һ�е����Ȼ�����Һ��������ɫ������֤������Һ��������Һ | |
| C�� | ij��ɫ��������ʯ����ĥ�������������ʹ��̪��Һ��ɺ�ɫ��֤���ù�������� | |
| D�� | ��ȼ�ŵ�ľ������ij��ɫ����ļ���ƿ�У�����Ϩ�𣬸�����һ���Ƕ�����̼���� |
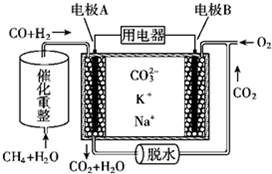
����˵������ȷ���ǣ�������
| A�� | ��ع���ʱ��K+��B���ƶ� | |
| B�� | �缫B�Ϸ����ĵ缫��Ӧ��O2+2CO2+4e-�T2CO32- | |
| C�� | ��ع���ʱ��CO2����ѭ������ | |
| D�� | ����1molCH4�������õ���CO��H2ͨ��缫A����Ҫ�缫Bͬʱͨ��33.6L��O2 |
��п��ϡ���ᷴӦ��ȡ������������������ͭ��Һ�ܼӿ췴Ӧ����
�ڶƲ������������п������������������������������ʴ
�۵��ʱ��Ӧ�Ѵ��ƽ������ڵ��۵�����
�ܵ�ⱥ���Ȼ�����Һ����ұ����������
�ݸ������泣����ʴ����Fe2O3•nH2O
��ͭ����ʱ��ͭ���ӵ�Դ������
�߽����ķ����У������������������������ñ�����������ԭ��صĸ�����
| A�� | �٢ڢۢݢޢ� | B�� | �٢ۢݢ� | C�� | �٢ۢݢ� | D�� | �٢ڢۢޢ� |
| A�� | ��Ȼ������Ҫ�ɷ� | B�� | װ�β�������Ƥ���� | ||
| C�� | �����ж� | D�� | ú���е���˹��ը |