题目内容
3.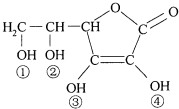 维生素C(VitaminC)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,其结构如图.下列有关说法中正确的是( )
维生素C(VitaminC)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,其结构如图.下列有关说法中正确的是( )| A. | 维生素C由于含有C═O键而能发生银镜反应 | |
| B. | 维生素C由于含有酯基而难溶于水 | |
| C. | 维生素C的分子式为C6H8O6 | |
| D. | 维生素C的酸性可能是①、②两个羟基引起的 |
分析 由结构简式可知分子式,分子中含碳碳双键、醇-OH、-COOC-,结合烯烃、醇、酯的性质来解答.
解答 解:A.不含-CHO,则不能发生银镜反应,故A错误;
B.含多个-OH,能溶于水,故B错误;
C.由结构简式可知,分子式为C6H8O6,故C正确;
D.羰基的氧是强吸电子的 故双键上的电子偏向羰基,从而③、④两个羟基上O吸引电子使氢离子易电离,显酸性,故D错误.
故选C.
点评 本题考查有机物的结构和性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重烯烃、醇、酯性质的考查,选项D为解答的难点,注意电子的偏移,题目难度不大.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
10.一未完成的离子方程式( )+XO${\;}_{3}^{-}$+6H+═( )3X2+3H2O,据此判断,氧化产物和还产物的物质的量之比为( )
| A. | 1:5 | B. | 3:1 | C. | 5:1 | D. | 7:1 |
11.在无色透明的溶液中,能大量共存的是( )
| A. | K+、Na+、NO3-、MnO4- | B. | Mg2+、Na+、Cl-、SO42- | ||
| C. | K+、Na+、Br-、Cu2+ | D. | Ca2+、Na+、Cl-、CO32- |
18.下列装置,可达到铁片上镀锌目的是( )
| A. |  含Fe2+电镀液 | B. | 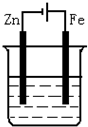 含Fe2+电镀液 | C. |  含Zn2+电镀液 | D. | 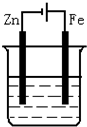 含Zn2+电镀液 |
8.等物质的量的主族金属A、B、C分别与足量的稀盐酸反应,所得氢气的体积依次为VA、VB、VC,已知2VB═VC,且VA═VB+VC,则在C的生成物中,该金属元素的化合价是( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
15.下列说法正确的是( )
| A. | 100mL、pH=3的HA和HB分别与足量的锌充分反应,HA放出的氢气多,说明HA的酸性比HB强 | |
| B. | 电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 | |
| C. | 在NH4HSO4溶液中由于的水解促进了水的电离,所以水的电离程度增大 | |
| D. | 在一密闭容器中发生2SO2+O2?2SO3反应,增大压强,平衡会正向移动,$\frac{{{c}^{2}(SO}_{3})}{{{{c}^{2}(SO}_{2})c(O}_{2})}$的值增大 |
12.下列物质不能通过化合反应得到的是( )
| A. | H2SiO3 | B. | Fe(OH)3 | C. | FeCl2 | D. | Fe3O4 |
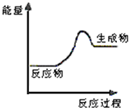 现有反应:A CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
现有反应:A CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑