��Ŀ����
9�� ij��ѧ��ѧ��ȤС��ͬѧΪ̽��Ԫ�������ɣ����������һϵ��ʵ�飮
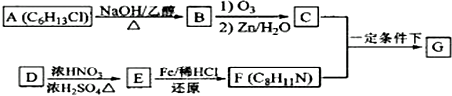
ij��ѧ��ѧ��ȤС��ͬѧΪ̽��Ԫ�������ɣ����������һϵ��ʵ�飮�����ʵ�����Ϊ1mol���ơ��ء�þ�����ֱ�Ͷ��������0.1mol•L-1�������У���Ԥ��ʵ������K�����ᷴӦ����ң�Al�����ᷴӦ������
��������ͼ��ʾװ�ÿ�����֤Ԫ�صķǽ����Եı仯���ɣ�
��1������A������Ϊ��Һ©��������D�������ǣ���ֹ����
��2����Ҫ֤���ǽ����ԣ�C��Si����A��Ӧ�������ᣬB��Ӧ����Na2CO3��C��Ӧ����Na2SiO3��Һ���۲쵽C�е�����Ϊ�а�ɫ��״����������
���� ��Ԫ�صĽ�����Խǿ���䵥�������ˮ��ӦԽ���ң�
II����1�����������Ĺ���д������A�����ƣ����θ���ܾ��з�ֹ���������ã�
��2��Ҫ֤���ǽ����ԣ�C��Si������ͨ��������̼�����Ʒ�Ӧ���������ԵĹ�����֤����
��� �⣺I��ͬһ����Ԫ�أ�����������ԭ�����������������Ԫ�صĽ�����Խǿ��ͬһ���壬ԭ������Խ������Խǿ���䵥�������ˮ��ӦԽ���ң����Խ�����K��Na��Mg��Al����K�����ᷴӦ����ҡ�Al�����ᷴӦ�����������ʴ�Ϊ��K��Al��
II����1������AΪ��Һ©�������θ����D�ܹ���ֹ���������Ա���C��Һ�������ƿ�У��ʴ�Ϊ����Һ©������ֹ������
��2����Ҫ֤���ǽ����ԣ�C��Si������ͨ��������̼�����Ʒ�Ӧ���������ԵĹ�����֤��������B�м�Na2CO3����A�п��Լ����ᣬͨ�������̼���Ƶķ�Ӧ����ȡCO2��Ȼ���CO2ͨ��C�е�Na2SiO3�У����Է�����Ӧ��Na2SiO3+CO2+H2O=H2SiO3��+Na2CO3��������ɫ��״�������Ӷ�����֤�����ԣ�H2CO3��H2SiO3���ʷǽ����ԣ�C��Si��
�ʴ�Ϊ�����Na2SiO3���а�ɫ��״����������
���� ���⿼������ʵ�鷽����ƣ��漰�������ǽ�����ǿ����̽������ȷ���ʵ������ǽⱾ��ؼ���֪�������ԡ��ǽ�����ǿ���жϷ���������������������ʵ�飬��Ŀ�Ѷ��еȣ�

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�| A�� | 0.5mol•L-1•min-1 | B�� | 1 mol•L-1•min-1 | ||
| C�� | 4 mol•L-1•min-1 | D�� | 2 mol•L-1•min-1 |
| A�� | ���� | B�� | ���� | C�� | ���� | D�� | һ����̼ |
| A�� | KCl���� | B�� | H2S���� | C�� | CCl4 | D�� | Mg |
| ʵ�鲽�� | ʵ������ |
| ��a��b���� | �����Ϊ����ɫ |
| ��c��d���� | �������� |
| ��c��e�ֱ�ͨ��������ˮ�� | �������ɫ������Һ |
| ��b��e�ֱ�ͨ���������� | ����������ɫ�Ļ��� |
| A�� | O2��NO��HCl��NH3��CO2 | B�� | O2��NO��NH3��HCl��SO2 | ||
| C�� | NO��O2��NH3��HCl��SO2 | D�� | HBr��Cl2��NH3��H2S��C2H4 |
| A�� | ������ | B�� | ����� | C�� | ������ | D�� | ���� |
| A�� | ��������������Һ��Ӧ����Al��OH��3��Na | |
| B�� | ���ڿ�����ȼ�����ɵ���ɫ��NaO2 | |
| C�� | ���ڸ�������ˮ������Ӧ����Fe3O4��H2 | |
| D�� | ��̼���ƺ��������Ʒ�Ӧ��NaHCO3 |
| A�� | 2SO2��g��+O2��g��$?_{500��}^{V_{2}O_{5}}$2SO3��g����H=-196.6kJ/mol����2molSO2��ȫ��Ӧ��ų���������196.6kJ | |
| B�� | ������ˮΪ֮��������ˮ��˵����ͬ������ˮ�ͱ��Ƚϣ����������� | |
| C�� | ��֪C��ʯī��=C�����ʯ����H=+1.9kJ/mol����������Ƕȿ����ʯ��ʯī�ȶ� | |
| D�� | ������ȼ����Ϊ285.8kJ/mol��������ȼ�յ��Ȼ�ѧ����ʽΪ2H2��g��+O2��g��=2H2O��l����H=-285.8kJ/mol |


 +HO-NO2$��_{��}^{ŨH_{2}SO_{4}}$
+HO-NO2$��_{��}^{ŨH_{2}SO_{4}}$ +H2O��
+H2O�� ��
�� ��д������һ�ֵĽṹ��ʽ����
��д������һ�ֵĽṹ��ʽ����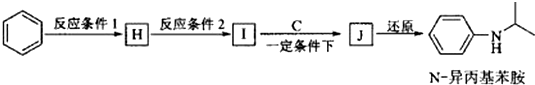
 ��
��