题目内容
16.有以下一系列反应,最终产物为草酸.已知B的相对分子质量比A的大79.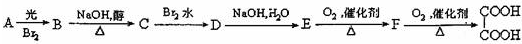
试回答下列问题:
(1)B的结构简式为CH3CH2Br,B→C的反应类型消去反应;
E→F的化学方程式:CH2OHCH2OH+O2$→_{△}^{Cu}$2H2O+OHC-CHO.
(2)由B发生水解反应或C与H2O发生加成反应均生成化合物G.在乙二酸、水、苯酚、G四种分子中,羟基上氢原子的活泼性由强到弱的顺序是(请用“>”将四种物质的化学式连接起来表示)HOOCCOOH>C6H5OH>H2O>CH3CH2OH.
(3)MTBE是一种重要的汽油添加剂,它是1-戊醇的同分异构体,又与G的某种同分异构体互为同系物,且分子中含有四个相同的烃基.则MTBE的结构简式为CH3-O-C(CH3)3,它的同类别同分异构体有6种(包括它本身).
分析 F被氧化生成乙二酸,则F是乙二醛,其结构简式为:OHCCHO,E被氧化生成乙二醛,则E是乙二醇,其结构简式为:CH2OHCH2OH,D和氢氧化钠水溶液发生取代反应生成乙二醇,C和溴发生加成反应生成D,则D是溴代烃;光照条件下,A和溴发生取代反应生成B,B是溴代烃,B的相对分子质量比A的大79,B发生消去反应生成C,C和溴发生加成反应生成D,则D的结构简式为:CH2BrCH2Br,C的结构简式为:CH2=CH2,B的结构简式为:CH3CH2Br,A的结构简式为:CH3CH3,据此分析解答.
解答 解:F被氧化生成乙二酸,则F是乙二醛,其结构简式为:OHCCHO,E被氧化生成乙二醛,则E是乙二醇,其结构简式为:CH2OHCH2OH,D和氢氧化钠水溶液发生取代反应生成乙二醇,C和溴发生加成反应生成D,则D是溴代烃;光照条件下,A和溴发生取代反应生成B,B是溴代烃,B的相对分子质量比A的大79,B发生消去反应生成C,C和溴发生加成反应生成D,则D的结构简式为:CH2BrCH2Br,C的结构简式为:CH2=CH2,B的结构简式为:CH3CH2Br,A的结构简式为:CH3CH3.
(1)通过以上分析知,B的结构简式为:CH3CH2Br,B发生消去反应生成C,则反应类型为消去反应,E→F是乙二醇被氧气氧化生成乙二醛,反应方程式为:CH2OHCH2OH+O2$→_{△}^{Cu}$2H2O+OHC-CHO,
故答案为:CH3CH2Br;消去反应;CH2OHCH2OH+O2$→_{△}^{Cu}$2H2O+OHC-CHO;
(2)乙二酸是羧酸酸性较强,苯酚弱酸性,故羟基上活泼氢原子的活泼性为乙二酸>苯酚>水>G(乙醇),
故答案为:HOOCCOOH>C6H5OH>H2O>CH3CH2OH;
(3)MTBE是一种重要的汽油添加剂,它是1戊醇的同分异构体,即分子式为C5H12O;又与G的某种同分异构体互为同系物,且分子中含有4个相同的烃基;则分子中5个碳原子有四个相同的基团应为甲基,故为CH3-O-C(CH3)3,其同类别同分异构体有甲丁醚4种,乙丙醚2种,共6种,
故答案为:CH3-O-C(CH3)3;6.
点评 本题考查了有机物的推断,以乙二酸为突破口采用逆推的方法进行推断,明确有机物的结构和性质是解本题关键,注意反应条件,反应条件不同导致产物不同,为易错点.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
| ①Fe(s)+CO2(g)?FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| ②Fe(s)+H2O(g)?FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
| ③CO(g)+H2O(g)?CO2(g)+H2(g) | K3 | ? | ? |
(1)反应①是吸热(填“吸热”或“放热”)反应.
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=$\frac{{K}_{2}}{{K}_{1}}$(用K1、K2表示).
(3)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有CE(填写字母序号).
A、缩小反应容器的容积 B、扩大反应容器的容积 C、升高温度
D、使用合适的催化剂 E、设法减小平衡体系中的CO的浓度
(4)若反应③的逆反应速率与时间的关系如图所示:
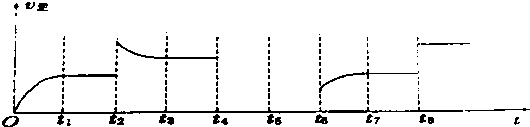
①可见反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的是什么条件:t2时增大生成物浓度或升高温度,t8时加入催化剂或加压.
②若t4时降压,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线.
 已知A、B、D、E均为中学化学常见物质,它们之间的转化关系如图所示(部分产物略去,①②③④的反应条件均相同).则A、E可能的组合为( )
已知A、B、D、E均为中学化学常见物质,它们之间的转化关系如图所示(部分产物略去,①②③④的反应条件均相同).则A、E可能的组合为( )①CO2、NaOH溶液;②Ca(HCO3)2溶液、Ca(OH)2溶液;③Na、O2;
④CuO、C;⑤AlCl3溶液、NH3•H2O ⑥NaAlO2溶液、盐酸.
| A. | ①③⑤ | B. | ①④⑤ | C. | ①④⑥ | D. | ①②⑥ |
| A. | 0.1 mol•L-1CH3COONa溶液与0.1 mol•L-1HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(H+) | |
| B. | 0.1 mol•L-1NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1 mol•L-1Na2CO3溶液与0.1 mol•L-1NaHCO3溶液等体积混合:$\frac{2}{3}$c(Na+)=c(CO32)+c(HCO3-)+c(H2CO3) | |
| D. | 0.1 mol•L-1Na2C2O4溶液与0.1 mol•L-1HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
数据编号 | 加入NaOH溶液的体积/mL | 溶液的pH | ||
| C(HX) | c(HY) | |||
| ① | 0 | 4 | 1 | |
| ② | a | 7 | ||
| ③ | 20.00 | x | y | |
| A. | 由表中数据可估算出25℃时Ka(HX)≈10-8 | |
| B. | 在相同温度下,物质的量浓度相同的两种酸溶液的导电能力为HX<HY | |
| C. | 编号②反应后的HY溶液中:c(Na+)>c(Y-)>c(OH-)>c(H+) | |
| D. | 编号③反应的溶液中:c(X-)>c(Y-) |
| A. | 氢氧化镭[Ra(OH2)]比氢氧化钙的碱性强 | |
| B. | 砹(At)的单质颜色为黑色 | |
| C. | 铍(Be)的原子失电子能力比镁弱 | |
| D. | 硒(Se)化氢比硫化氢稳定 |
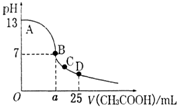 室温下,在25mL 0.1mol.L-1NaOH溶液中逐滴加入0.2mol•L-1 CH3COOH 溶液,pH 与滴加 CH3COOH溶液体积的关系曲线如图所示,若忽略两溶液混合时的体积变化,下列有关粒子浓度关系的说法错误的是( )
室温下,在25mL 0.1mol.L-1NaOH溶液中逐滴加入0.2mol•L-1 CH3COOH 溶液,pH 与滴加 CH3COOH溶液体积的关系曲线如图所示,若忽略两溶液混合时的体积变化,下列有关粒子浓度关系的说法错误的是( )
