题目内容
10.对于合成氨反应,N2(g)+3H2(g)?2NH3(g)△H<0.达到平衡后,以下分析正确的是( )| A. | 升高温度,对正反应的反应速率影响更大 | |
| B. | 增大压强,对正反应的反应速率影响更大 | |
| C. | 减小反应物浓度,对逆反应的反应速率影响更大 | |
| D. | 加入催化剂,对逆反应的反应速率影响更大 |
分析 A.升高温度正逆反应速率都增大,平衡向逆反应方向移动,说明温度对逆反应速率影响较大;
B.增大压强,平衡正向移动,则压强对正反应速率影响较大;
C.减小反应物浓度,逆反应速率不变;
D.加入催化剂,对正逆反应速率影响相同.
解答 解:A.该反应的正反应是放热反应,升高温度正逆反应速率都增大,但平衡向逆反应方向移动,说明温度对逆反应速率影响较大,故A错误;
B.该反应的正反应是反应前后气体体积减小的反应,增大压强,平衡正向移动,则压强对正反应速率影响较大,故B正确;
C.减小反应物浓度,生成物浓度不变,则逆反应速率不变,故C错误;
D.加入催化剂,对正逆反应速率影响相同,所以正逆反应速率仍然相等,故D错误;
故选B.
点评 本题考查化学反应速率影响因素,为高频考点,明确外界条件对化学平衡影响原理是解本题关键,注意结合反应特点分析,注意:催化剂影响反应速率但不影响平衡移动.

练习册系列答案
相关题目
20.关于0.1mol/LNa2S水溶液中的下列关系式,正确的是( )
①c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
②c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-)
③c(Na+)=2c(S2-)+2c(H2S)+2c(HS-)
④c(OH-)=c(HS-)+c(H+)+2c(H2S)
①c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
②c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-)
③c(Na+)=2c(S2-)+2c(H2S)+2c(HS-)
④c(OH-)=c(HS-)+c(H+)+2c(H2S)
| A. | 仅① | B. | 仅①② | C. | 仅①②③ | D. | ①②③④ |
18.下列说法正确的是( )
| A. | 糖类物质都有甜味 | B. | 糖类物质的组成都符合通式Cm(H2O)n | ||
| C. | 动植物的生命活动都需要糖 | D. | 糖类都能发生水解反应 |
15.常温下,将某一元碱BOH和HCl溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答:
(1)从第①组情况分析,BOH是弱碱(选填“强碱”或“弱碱”).该组所得混合溶液中由水电离出的c(H+)=1×10-5mol•L-1.
(2)第②组情况表明,c<0.2.该混合液中离子浓度c(B+)=c(Cl-)(选填“<”、“>”或“=”).
(3)从第③组实验结果分析,混合溶液中 (选填“<”、“>”或“=”)
甲:BOH的电离程度>BCl的水解程度
乙:混合溶液中的离子浓度由大到小的顺序c(B+)>c(Cl-)>c(OH-)>c(H+).
| 实验编号 | HCl的物质的量浓度 (mol•L-1) | BOH的物质的量浓度 (mol•L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=5 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.1 | 0.2 | pH>7 |
(1)从第①组情况分析,BOH是弱碱(选填“强碱”或“弱碱”).该组所得混合溶液中由水电离出的c(H+)=1×10-5mol•L-1.
(2)第②组情况表明,c<0.2.该混合液中离子浓度c(B+)=c(Cl-)(选填“<”、“>”或“=”).
(3)从第③组实验结果分析,混合溶液中 (选填“<”、“>”或“=”)
甲:BOH的电离程度>BCl的水解程度
乙:混合溶液中的离子浓度由大到小的顺序c(B+)>c(Cl-)>c(OH-)>c(H+).
2.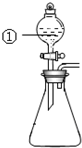 用如图所示装置进行下列实验:将①中溶液滴入锥形瓶中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入锥形瓶中,预测的现象与实际相符的是( )
 用如图所示装置进行下列实验:将①中溶液滴入锥形瓶中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入锥形瓶中,预测的现象与实际相符的是( )| 选项 | ①中物质 | 锥形瓶中物质 | 预测锥形瓶中的现象 |
| A | 浓盐酸 | “84”消毒液 | 有黄绿色气体产生 |
| B | 浓硝酸 | 光洁的铁钉 | 产生红棕色气体 |
| C | 氯化铝溶液 | 浓氢氧化钠溶液 | 先有白色沉淀生成, 后沉淀又溶解 |
| D | 草酸溶液 | 酸性高锰酸钾溶液 | 溶液逐渐褪色, 有黑色沉淀生成 |
| A. | A | B. | B | C. | C | D. | D |
19.下列有机物分子中,存在顺反异构的是( )
| A. | 2,3二溴丙烯 | B. | 2,3二甲基-2-丁烯 | ||
| C. | 丙烯 | D. | 2-丁烯 |
20.下列实验操作不可以实现实验目的是( )
| A. | 除去乙酸乙酯中混有的乙酸,可以加入Na2CO3溶液,再分液 | |
| B. | 将SO2通入滴有酚酞的NaOH溶液中,溶液褪色,可以证明SO2具有漂白性 | |
| C. | 用金属钠分别与水和乙醇反应,可比较水分子中氢原子和乙醇羟基中氢原子的活泼性 | |
| D. | 先加盐酸酸化,再加入BaCl2溶液,生成白色沉淀,可确定该溶液中含有SO42- |