题目内容
19.标准状况下,22.4L己烷中含共价键数目为19NA.× (判断对错)分析 标准状况下,己烷为液体,不能用气体摩尔体积计算,以此解答.
解答 解:标准状况下,己烷为液体,不能用气体摩尔体积计算,则22.4L己烷中含共价键数目不是19NA.故答案为:×.
点评 本题考查物质的量的相关计算和判断,为高频考点,侧重于学生的分析、计算能力的考查,难度不大,注意气体摩尔体积的使用范围.

练习册系列答案
相关题目
9.(1)在短周期主族元素中,氯及其相邻两元素的电负性由大到小的顺序是F>Cl>S(用元素符号表示)
(2)A、B、C为同一短周期金属元素.依据下表数据分析,C元素在化合物中的主要化合价为+3;A、B、C三种元素的原子半径由大到小的顺序是A>B>C.
(3)已知过氧化氢分子的空间结构如图所示,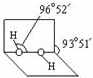 分子中氧原子采取sp3杂化;通常情况下,H2O2与水任意比互溶的主要原因是H2O2分子与水分子间形成氢键,使H2O2与水任意比互溶.
分子中氧原子采取sp3杂化;通常情况下,H2O2与水任意比互溶的主要原因是H2O2分子与水分子间形成氢键,使H2O2与水任意比互溶.
(4)R是1~36号元素中未成对电子数最多的原子.R3+在溶液中存在如下转化:
R3+$?_{H+}^{OH-}$R(OH)3$?_{H+}^{OH-}$[R(OH)4]-
①基态R原子的价电子排布式为3d54s1.
②[R(OH)4]-中存在的化学键是BD.
A.离子键 B.极性键 C.非极性键 D.配位键
(5)等电子体原理可广义理解为:重原子数相等(重原子指原子序数≥4的原子),总电子数或价电子数相等的分子或离子.若将H2O2滴入液氨中,可得白色固体A,红外光谱显示,A中有阴阳两种离子,阳离子是正四面体,阴离子与H2O2互为等电子体.则A的结构简式为NH4OOH.
(2)A、B、C为同一短周期金属元素.依据下表数据分析,C元素在化合物中的主要化合价为+3;A、B、C三种元素的原子半径由大到小的顺序是A>B>C.
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 500 | 4600 | 6900 | 9500 |
| B | 740 | 1500 | 7700 | 10500 |
| C | 580 | 1800 | 2700 | 11600 |
 分子中氧原子采取sp3杂化;通常情况下,H2O2与水任意比互溶的主要原因是H2O2分子与水分子间形成氢键,使H2O2与水任意比互溶.
分子中氧原子采取sp3杂化;通常情况下,H2O2与水任意比互溶的主要原因是H2O2分子与水分子间形成氢键,使H2O2与水任意比互溶.(4)R是1~36号元素中未成对电子数最多的原子.R3+在溶液中存在如下转化:
R3+$?_{H+}^{OH-}$R(OH)3$?_{H+}^{OH-}$[R(OH)4]-
①基态R原子的价电子排布式为3d54s1.
②[R(OH)4]-中存在的化学键是BD.
A.离子键 B.极性键 C.非极性键 D.配位键
(5)等电子体原理可广义理解为:重原子数相等(重原子指原子序数≥4的原子),总电子数或价电子数相等的分子或离子.若将H2O2滴入液氨中,可得白色固体A,红外光谱显示,A中有阴阳两种离子,阳离子是正四面体,阴离子与H2O2互为等电子体.则A的结构简式为NH4OOH.
7.合金是一类用途广泛的金属材料.下列物质中,不属于合金的是( )
| A. | 黄铜 | B. | 钢 | C. | 水银 | D. | 硬铝 |
14.下列说法正确的是( )
| A. | 合成纤维、人造纤维及碳纤维都属于有机高分子材料 | |
| B. | KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 | |
| C. | SO2、SiO2、CO均为酸性氧化物 | |
| D. | 福尔马林、水玻璃、氨水均为混合物 |
8.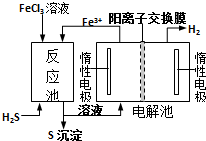 现代工业生产中常用电解氯化亚铁的方法制得氯化铁溶液,吸收有毒的硫化氢气体.工艺原理如图所示.下列说法中正确的是( )
现代工业生产中常用电解氯化亚铁的方法制得氯化铁溶液,吸收有毒的硫化氢气体.工艺原理如图所示.下列说法中正确的是( )
 现代工业生产中常用电解氯化亚铁的方法制得氯化铁溶液,吸收有毒的硫化氢气体.工艺原理如图所示.下列说法中正确的是( )
现代工业生产中常用电解氯化亚铁的方法制得氯化铁溶液,吸收有毒的硫化氢气体.工艺原理如图所示.下列说法中正确的是( )| A. | 电解池中OH-从右槽迁移到左槽 | |
| B. | H+在右槽发生氧化反应 | |
| C. | 左槽中发生的反应是:4OH--4e-═O2↑+2H2O | |
| D. | 常温常压下,反应中每转移1mol电子生成1g氢气 |
9.化学与生活密切相关,下列有关说法正确的是( )
| A. | 维生素C具有还原性,在人体内起抗氧化作用 | |
| B. | 淀粉、油脂和蛋白质都是高分子化合物 | |
| C. | 煤经气化和液化两个物理变化过程,可变为清洁能源 | |
| D. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是有机高分子材料 |