题目内容
10.下列叙述正确的是( )| A. | HF、HCl、HBr、HI的熔点沸点依次升高 | |
| B. | 氯的各种含氧酸的酸性由强到弱排列为HClO4<HClO3<HClO2<HClO | |
| C. | 元素的性质呈现周期性变化的根本原因是元素原子的核外电子排布呈周期性变化 | |
| D. | 稀有气体一般难于发生化学反应,是由于其键能大 |
分析 A.HF分子之间存在氢键,故熔点沸点相对较高;
B.同一元素若能形成几种不同氧化态的含氧酸,其酸性随化合价递增而递增;
C.根据“结构决定性质”分析;
D.稀有气体为单原子分子,原子都形成稳定结构.
解答 解:A.HF分子之间存在氢键,故熔点沸点相对较高,故熔点沸点的大小关系为HF>HI>HBr>HCl,故A错误;
B.同一元素若能形成几种不同氧化态的含氧酸,其酸性随化合价递增而递增,故酸性为HClO4>HClO3>HClO2>HClO,故B错误;
C.元素原子的核外电子排布呈周期性变化导致元素的性质呈现周期性变化,故C正确;
D.稀有气体为单原子分子,原子都形成稳定结构,稀有气体一般难于发生化学反应,与键能无关,故D错误;
故选C.
点评 本题考查氢键的存在及对物质性质色影响、同一元素形成的不同含氧酸的酸性大小判断,难度不大.要注意氢键对物质熔沸点的影响.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.某烷烃的相对分子质量为72,跟氯气发生取代反应所得的一氯取代物没有同分异构体,这种烷烃是( )
| A. | CH3CH2CH2CH2CH3 | B. | 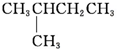 | C. |  | D. | 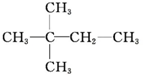 |
18.下列物质能促进水的电离的是( )
| A. | 碳酸钠 | B. | 醋酸 | C. | 乙醇 | D. | 氯化钠 |
5. 苯甲酸(无色针状晶体,熔点122.4℃)可广泛用于医药、染料载体、香料等,实验室用甲苯和高锰酸钾制备苯甲酸.反应方程式如下:
苯甲酸(无色针状晶体,熔点122.4℃)可广泛用于医药、染料载体、香料等,实验室用甲苯和高锰酸钾制备苯甲酸.反应方程式如下:
 +2KMnO4 $\stackrel{△}{→}$
+2KMnO4 $\stackrel{△}{→}$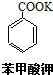 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O
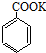 +HCl→
+HCl→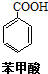 +KCl
+KCl
已知有关化合物的相关数据如表所示:
苯甲酸在100g水中的溶解度:0.18g(4℃),0.27g(18℃),2.2g(75℃).
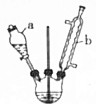
合成:如图(固定及加热装置略去)所示,在三颈烧瓶中加入4.23mL甲苯和100mL蒸馏水,瓶口装上温度计、电动搅拌器、冷凝管,慢慢开启电动搅拌器,加热至沸腾.经冷凝管上口分批加入21.30g高锰酸钾(过量),继续煮沸至甲苯层消失,回流液中不再出现油珠为止,得到反应混合物.
对反应混合物进行分离:①趁热过滤→②洗涤滤渣→③合并滤液和洗涤液→④冷却→⑤盐酸酸化→⑥过滤.
对粗产品苯甲酸进行提纯:①沸水溶解→②活性炭脱色→③趁热过滤→④冷却结晶→⑤过滤→⑥洗涤→⑦干燥.
请回答下列有关问题:
(1)实验中准确量取4.23mL甲苯所需仪器为酸式滴定管.
(2)冷凝管的上口是否需要塞上塞子否(填“是”或“否”),a处水流方向是进水(填“进水”或“出水”).
(3)高锰酸钾需要分批加入,请用化学反应速率观点说明理由避免反应过快,使反应液从回流管上端喷.
(4)在对粗产品苯甲酸进行提纯过程中,“③趁热过滤”的目的是除去活性炭,减少苯甲酸结晶析出;“④”的操作名称是冷却结晶;可证明“⑥洗涤”步骤已洗涤干净的方法是取最后一次洗涤液,加入用HNO3酸化的AgNO3溶液,若无白色沉淀生成,说明沉淀已洗涤干净.
(5)干燥后称量得苯甲酸2.93g,则苯甲酸的产率为60%.
 苯甲酸(无色针状晶体,熔点122.4℃)可广泛用于医药、染料载体、香料等,实验室用甲苯和高锰酸钾制备苯甲酸.反应方程式如下:
苯甲酸(无色针状晶体,熔点122.4℃)可广泛用于医药、染料载体、香料等,实验室用甲苯和高锰酸钾制备苯甲酸.反应方程式如下: +2KMnO4 $\stackrel{△}{→}$
+2KMnO4 $\stackrel{△}{→}$ +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O  +HCl→
+HCl→ +KCl
+KCl已知有关化合物的相关数据如表所示:
| 化合物 | 相对分子质量 | 密度(g•cm-3) | 溶解性 | 沸点(℃) |
| 甲苯 | 92 | 0.87 | 难溶于水 | 110.0 |
| 苯甲酸钾 | 160 | - | 易溶于水 | - |
| 苯甲酸 | 122 | 1.26 | 微溶于水 | 248.0 |
合成:如图(固定及加热装置略去)所示,在三颈烧瓶中加入4.23mL甲苯和100mL蒸馏水,瓶口装上温度计、电动搅拌器、冷凝管,慢慢开启电动搅拌器,加热至沸腾.经冷凝管上口分批加入21.30g高锰酸钾(过量),继续煮沸至甲苯层消失,回流液中不再出现油珠为止,得到反应混合物.
对反应混合物进行分离:①趁热过滤→②洗涤滤渣→③合并滤液和洗涤液→④冷却→⑤盐酸酸化→⑥过滤.
对粗产品苯甲酸进行提纯:①沸水溶解→②活性炭脱色→③趁热过滤→④冷却结晶→⑤过滤→⑥洗涤→⑦干燥.
请回答下列有关问题:
(1)实验中准确量取4.23mL甲苯所需仪器为酸式滴定管.
(2)冷凝管的上口是否需要塞上塞子否(填“是”或“否”),a处水流方向是进水(填“进水”或“出水”).
(3)高锰酸钾需要分批加入,请用化学反应速率观点说明理由避免反应过快,使反应液从回流管上端喷.
(4)在对粗产品苯甲酸进行提纯过程中,“③趁热过滤”的目的是除去活性炭,减少苯甲酸结晶析出;“④”的操作名称是冷却结晶;可证明“⑥洗涤”步骤已洗涤干净的方法是取最后一次洗涤液,加入用HNO3酸化的AgNO3溶液,若无白色沉淀生成,说明沉淀已洗涤干净.
(5)干燥后称量得苯甲酸2.93g,则苯甲酸的产率为60%.
19.在温度不变的条件下,在恒容的容器中进行下列反应:N2O4(g)═2NO2(g),若N2O4的浓度由0.1mol•L-1降到0.07mol•L-1需要15s,那么N2O4的浓度由0.07mol•L-1降到0.05mol•L-1所需的反应时间( )
| A. | 等于5s | B. | 等于10s | C. | 小于10s | D. | 大于10s |
20.某航空站安装了一台燃料电池,该电池可同时提供电和水蒸气,所用燃料为氢气,电解质为熔融的碳酸钾.已知电池的总反应为2H2+O2=2H2O,正极反应为O2+2CO2+4e-=2CO32-.下列说法正确的是( )
| A. | 该电池可在常温或高温时工作,对环境有较强的适应性 | |
| B. | 负极反应为H2+2OH--2e-=2H2O | |
| C. | 该电池工作时负极有CO2生成 | |
| D. | 该电池供应2molH2O,同时转移2mol电子 |
 己二酸是合成高分子化合物尼龙-66的原料.某学习小组拟在实验室以环己醇为原料制备己二酸.反应原理如下:
己二酸是合成高分子化合物尼龙-66的原料.某学习小组拟在实验室以环己醇为原料制备己二酸.反应原理如下: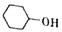 +8HNO3$\stackrel{一定条件}{→}$3HOOC(CH3)4COOH+8NO↑+7H2O
+8HNO3$\stackrel{一定条件}{→}$3HOOC(CH3)4COOH+8NO↑+7H2O ;
; ;
;