题目内容
某化学兴趣小组要完成中和热的测定.
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol?L-1
盐酸、0.55mol?L-1NaOH溶液,实验尚缺少的玻璃用品是 、 .
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”),其原因是
(3)他们记录的实验数据如下:
已知:Q=c m(t2-t1),反应后溶液的比热容c为4.18kJ?℃-1?kg-1,各物质的密度均为1g?cm-3.
①计算完成上表.
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式: .
(4)若用KOH代替NaOH,对测定结果 (填“有”或“无”)影响;若用醋酸代替HCl做实验,对测 定结果 (填“有”或“无”)影响.
(5)已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,回答下列问题.
①用含20g NaOH的稀溶液跟足量稀盐酸反应放出 kJ的热量.
②用含2mol H2SO4的稀溶液跟足量稀NaOH反应,此反应的中和热△H为 .
③如果将?反应中的稀盐酸换成稀醋酸,反应放出的热量 (填“大于”、“小于”或“等于”)?放出的热量.
(1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5mol?L-1
盐酸、0.55mol?L-1NaOH溶液,实验尚缺少的玻璃用品是
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?
(3)他们记录的实验数据如下:
| 实验用品 | 溶液温度 | 中和热 | |||
| t1 | t2 | △H | |||
| ① | 50 mL 0.55 mol?L-1 NaOH溶液 | 50 mL 0.5 mol?L-1 HCl溶液 | 20℃ | 23.3℃ | |
| ② | 50 mL 0.55 mol?L-1 NaOH溶液 | 50 mL 0.5 mol?L-1 HCl溶液 | 20℃ | 23.5℃ | |
①计算完成上表.
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:
(4)若用KOH代替NaOH,对测定结果
(5)已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,回答下列问题.
①用含20g NaOH的稀溶液跟足量稀盐酸反应放出
②用含2mol H2SO4的稀溶液跟足量稀NaOH反应,此反应的中和热△H为
③如果将?反应中的稀盐酸换成稀醋酸,反应放出的热量
考点:中和热的测定
专题:实验设计题
分析:(1)根据各仪器的作用结合中和热实验原理来选取仪器;
(2)金属导热快,热量损失多;
(3)先判断温度差的有效性,然后求出温度差平均值,再根据Q=m?c?△T计算反应放出的热量,然后根据△H=-
kJ/mol计算出反应热,根据中和热的概念以及热化学方程式的书写方法写出热化学方程式;
(4)根据中和热的概念分析,弱电解质电离吸热;
(5)①根据H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ?mol-1可知,生成1molH2O放出热量为57.3kJ,然后根据水的物质的量与热量成正比求出热量即可;
②根据中和热的概念:稀的强酸和强碱反应生成1mol水所放出的热量求出中和热,和参加反应的量无关;
③根据弱电解质的电离吸热来分析.
(2)金属导热快,热量损失多;
(3)先判断温度差的有效性,然后求出温度差平均值,再根据Q=m?c?△T计算反应放出的热量,然后根据△H=-
| Q |
| n |
(4)根据中和热的概念分析,弱电解质电离吸热;
(5)①根据H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ?mol-1可知,生成1molH2O放出热量为57.3kJ,然后根据水的物质的量与热量成正比求出热量即可;
②根据中和热的概念:稀的强酸和强碱反应生成1mol水所放出的热量求出中和热,和参加反应的量无关;
③根据弱电解质的电离吸热来分析.
解答:
解:(1)测定稀盐酸和稀氢氧化钠的中和热,所需要的玻璃仪器有:大、小两个烧杯、胶头滴管、量筒、温度计以及环形玻璃搅拌器,需要用量筒量取酸溶液、碱溶液的体积,需要使用温度计测量温度,所以还缺少温度计和量筒;
故答案为:量筒;温度计;
(2)不能用环形铜丝搅拌棒代替环形玻璃搅拌棒,因为铜丝搅拌棒是热的良导体,热量损失大,
故答案为:否;金属易导热,热量散失导致误差大;
(3)2次温度差分别为:3.3℃,3.5℃,2组数据都有效,温度差平均值=3.4℃,50mL0.55mol?L-1NaOH和50mL.0.5mol?L-1HCl质量和为m=100mL×1g/mL=100g,c=4.18J/(g?℃),△T=3.4℃,代入公式Q=cm△T得生成0.025mol的水放出热量Q=4.18J/(g?℃)×100g×3.4℃=1421.2J=1.4212KJ,即生成0.025mol的水放出热量1.4212KJ,所以生成1mol的水放出热量为
=56.8kJ,即该实验测得的中和热△H=-56.8kJ/mol,NaOH溶液与HCl溶液反应的热化学方程式为:HCl(aq)+NaOH(aq)=NaCl(aq)+2H2O(l)△H=-56.8kJ/mol,
故答案为:-56.8kJ/mol;HCl(aq)+NaOH(aq)=NaCl(aq)+2H2O(l)△H=-56.8kJ/mol;
(4)在稀溶液中,酸跟碱发生中和反应生成1mol水时的反应热叫做中和热,若用KOH代替NaOH,测定结果无影响,醋酸为弱酸,电离过程为吸热过程,所以用醋酸代替HCl做实验,反应放出的热量小于56.8kJ,测定结果偏小,对测定结果有影响,
故答案为:无;有;
(5)①H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ?mol-1可知,生成1molH2O放出热量为57.3kJ,
20gNaOH即0.5mol氢氧化钠配成稀溶液后,氢氧根离子的浓度是0.5mol,和足量的酸之间反应会生成0.5mol水,所以放出热量为0.5×57.3kJ=28.65kJ,
故答案为:28.65;
②用2molH2SO4配稀溶液跟足量稀NaOH反应,会生成水4mol,所以放出热量为4×57.3kJ=229.2kJ,但中和热指稀的强酸和强碱反应生成1mol水所放出的热量,所以中和热和参加反应的量无关,此反应的中和热△H为为=-57.3kJ/mol,
故答案为:-57.3kJ/mol;
③由于醋酸是弱酸,电离是吸热的,所以导致放出的热量数值偏低,
故答案为:小于;
故答案为:量筒;温度计;
(2)不能用环形铜丝搅拌棒代替环形玻璃搅拌棒,因为铜丝搅拌棒是热的良导体,热量损失大,
故答案为:否;金属易导热,热量散失导致误差大;
(3)2次温度差分别为:3.3℃,3.5℃,2组数据都有效,温度差平均值=3.4℃,50mL0.55mol?L-1NaOH和50mL.0.5mol?L-1HCl质量和为m=100mL×1g/mL=100g,c=4.18J/(g?℃),△T=3.4℃,代入公式Q=cm△T得生成0.025mol的水放出热量Q=4.18J/(g?℃)×100g×3.4℃=1421.2J=1.4212KJ,即生成0.025mol的水放出热量1.4212KJ,所以生成1mol的水放出热量为
| 1.4212KJ×1mol |
| 0.025mol |
故答案为:-56.8kJ/mol;HCl(aq)+NaOH(aq)=NaCl(aq)+2H2O(l)△H=-56.8kJ/mol;
(4)在稀溶液中,酸跟碱发生中和反应生成1mol水时的反应热叫做中和热,若用KOH代替NaOH,测定结果无影响,醋酸为弱酸,电离过程为吸热过程,所以用醋酸代替HCl做实验,反应放出的热量小于56.8kJ,测定结果偏小,对测定结果有影响,
故答案为:无;有;
(5)①H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ?mol-1可知,生成1molH2O放出热量为57.3kJ,
20gNaOH即0.5mol氢氧化钠配成稀溶液后,氢氧根离子的浓度是0.5mol,和足量的酸之间反应会生成0.5mol水,所以放出热量为0.5×57.3kJ=28.65kJ,
故答案为:28.65;
②用2molH2SO4配稀溶液跟足量稀NaOH反应,会生成水4mol,所以放出热量为4×57.3kJ=229.2kJ,但中和热指稀的强酸和强碱反应生成1mol水所放出的热量,所以中和热和参加反应的量无关,此反应的中和热△H为为=-57.3kJ/mol,
故答案为:-57.3kJ/mol;
③由于醋酸是弱酸,电离是吸热的,所以导致放出的热量数值偏低,
故答案为:小于;
点评:本题考查中和热的测定,题目难度不大,注意热量计算公式的应用中c=4.18J/(g?℃),要注意热量单位的换算,注意中和热的定义.

练习册系列答案
相关题目
下列装置所示的实验中,能达到实验目的是( )
A、 除去Cl2中的HCl |
B、 防止地下钢管腐蚀 |
C、 分离酒精和水 |
D、 电解精炼铜 |
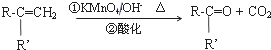
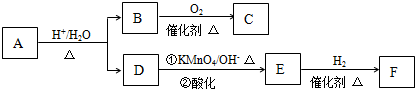
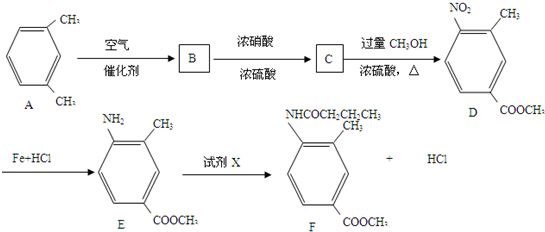
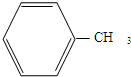 制备化合物
制备化合物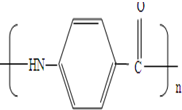
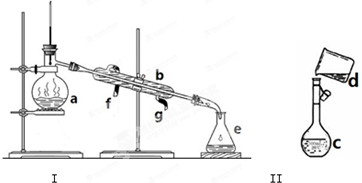 掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置.
掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为两套实验装置. 如图为实验室某浓硫酸试剂瓶上的标签,回答有关问题:
如图为实验室某浓硫酸试剂瓶上的标签,回答有关问题: