题目内容
 室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可按框图进行反应.又知D溶液为黄色,E溶液是无色的,请回答:
室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可按框图进行反应.又知D溶液为黄色,E溶液是无色的,请回答:(1)D的化学式是
(2)反应④的化学方程式为
(3)现有12mol/L的E溶液,要稀释为0.15mol/L的稀溶液480mL,需要的仪器除烧杯、玻璃棒、量筒、胶头滴管、还需要
考点:无机物的推断
专题:推断题
分析:由B为黄绿色气体且为单质,可知B为Cl2;由框图可知反应生成的固体D为固体单质A与Cl2反应生成的一种氯化物;反应生成的E为Cl2与气体单质C生成的一种可溶于水的氯化物,且E溶液和固体单质A又可以重新生成气体C和F,只有当C为H2,F为一种氯化物时才能满足这一过程;而A与Cl2反应已生成了一种氯化物D,F又是一种氯化物,所以A为变价金属,应为Fe,所以A为Fe,B为Cl2,C为H2,D为FeCl3,E为HCl,F为FeCl2,结合物质的相关性质解答该题.
解答:
解:由B为黄绿色气体且为单质,可知B为Cl2;由框图可知反应生成的固体D为固体单质A与Cl2反应生成的一种氯化物;反应生成的E为Cl2与气体单质C生成的一种可溶于水的氯化物,且E溶液和固体单质A又可以重新生成气体C和F,只有当C为H2,F为一种氯化物时才能满足这一过程;而A与Cl2反应已生成了一种氯化物D,F又是一种氯化物,所以A为变价金属,应为Fe,所以A为Fe,B为Cl2,C为H2,D为FeCl3,E为HCl,F为FeCl2,
(1)由以上分析可知D为FeCl3,B为Cl2,Cl原子核外有17个电子,其原子结构示意图为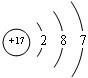 ,
,
故答案为:FeCl3; ;
;
(2)反应④为FeCl2和Cl2的反应,反应的化学方程式为2FeCl2+Cl2=2FeCl3,
故答案为:2FeCl2+Cl2=2FeCl3;
(3)实验室没有480mL容量瓶,应配制成500mL,则n(HCl)=0.15mol/L×0.5L=0.075mol,需要浓盐酸的体积为
=0.0063L=6.3mL,
在配置过程中如果定容时俯视刻度线,会呆滞溶液体积偏小,则会造成所配溶液浓度偏大,实验时,量筒不需要洗涤,不洗涤对实验结果没有影响.
故答案为:500mL容量瓶;6.3;偏高;无影响.
(1)由以上分析可知D为FeCl3,B为Cl2,Cl原子核外有17个电子,其原子结构示意图为
 ,
,故答案为:FeCl3;
 ;
;(2)反应④为FeCl2和Cl2的反应,反应的化学方程式为2FeCl2+Cl2=2FeCl3,
故答案为:2FeCl2+Cl2=2FeCl3;
(3)实验室没有480mL容量瓶,应配制成500mL,则n(HCl)=0.15mol/L×0.5L=0.075mol,需要浓盐酸的体积为
| 0.075mol |
| 12mol/L |
在配置过程中如果定容时俯视刻度线,会呆滞溶液体积偏小,则会造成所配溶液浓度偏大,实验时,量筒不需要洗涤,不洗涤对实验结果没有影响.
故答案为:500mL容量瓶;6.3;偏高;无影响.
点评:本题考查无机物的推断,涉及Fe、Cl元素单质及其化合物性质等,注意根据物质的颜色作为突破口,再结合转化关系推断,难度不大,侧重对常用化学用语的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
镍镉电池在通讯、交通及日常生活中有着广泛的应用,其工作原理可以表示为:
Cd+2NiO(OH)(s)+2H2O?2Ni(OH)2(s)+Cd(OH)2(s)
(以强碱为电解质)以下说法中正确的是( )
Cd+2NiO(OH)(s)+2H2O?2Ni(OH)2(s)+Cd(OH)2(s)
(以强碱为电解质)以下说法中正确的是( )
| A、以上反应是可逆反应 |
| B、放电时,镉为正极 |
| C、放电时负极附近溶液的pH不变 |
| D、充电时阳极发生氧化反应 |
过滤时正确的操作为( )
| A、将待过滤的物质搅拌后直接倒入过滤器中 |
| B、将待过滤的物质静置后先倒出上层清液,再将沉淀倒入过滤器中 |
| C、将待过滤的物质静置后直接倒入过滤器中 |
| D、将待过滤的物质沿着玻璃棒倒入过滤器中,玻璃棒下端应靠在三层滤纸处 |
 在如图装置中,通电后可观察到Cu极溶解,则下列说法中不正确的是( )
在如图装置中,通电后可观察到Cu极溶解,则下列说法中不正确的是( )| A、直流电源中,A是正极 |
| B、两池内CuSO4溶液浓度均不改变 |
| C、两池中的铁电极上最初析出物质相同 |
| D、P池内溶液的质量逐渐减小 |
下列各组物质间反应可能包括多步反应,其总的离子方程式正确的是( )
| A、等体积、等物质的量浓度的明矾溶液和Ba(OH)2溶液混合:3Ba2++6OH -+2Al3++3SO42-═2Al(OH)3↓+3BaSO4↓ |
| B、FeSO4酸性溶液暴露在空气中:4Fe2++O2+2H2O=4Fe3++4OH - |
| C、向AlCl3溶液中投入过量Na:2Al3++6Na+6H2O=2Al(OH)3↓+6Na++3H2↑ |
| D、向FeBr2 溶液中通入少量Cl2:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
下列说法正确的是( )
| A、金属单质在反应中只能作还原剂,非金属单质只能作氧化剂 |
| B、失电子多的金属还原性强 |
| C、某元素从化合态到游离态,该元素一定被还原 |
| D、氧化还原反应中一定存在电子的转移 |

