题目内容
4.关于二氧化硫的下列说法中,不正确的是( )| A. | SO2是硫及其某些硫化物在空气中燃烧的产物 | |
| B. | SO2具有漂白作用,也有防腐作用 | |
| C. | SO2是硫酸的酸酐,称为硫酐 | |
| D. | SO2是一种大气污染物 |
分析 二氧化硫为酸性氧化物,具有漂白性,为无色有刺激性气体有毒气体,以此解答该题.
解答 解:A.硫及某些含硫化合物在空气中燃烧可生成二氧化硫,故A正确;
B.二氧化硫具有漂白性,可用于工业漂白,二氧化硫溶于水,生成亚硫酸为强还原剂,能阻断微生物的生理氧化过程,对细菌、霉菌、酵母菌均有抑制作用,故其既是漂白剂又是防腐剂,故B正确;
C.二氧化硫与水反应生成亚硫酸,SO2是亚硫酸的酸酐,故C错误;
D.二氧化硫有毒,可导致酸雨,为大气污染物,故D正确.
故选C.
点评 本题考查了元素化合物知识,侧重考查二氧化硫的性质,熟悉二氧化硫的漂白性、酸性氧化物的性质是解题关键,注意酸雨形成原因,难度不大.

练习册系列答案
相关题目
14.下列实验过程中,始终看不到明显变化的是( )
| A. | 向10mL0.1mol/LFeCl2溶液中缓缓通入标准状况下11.2mLCl2 | |
| B. | 向AlC13溶液中滴加Na2S溶液 | |
| C. | 向含有Na+、Fe2+、Cl-、SO42-的溶液中通入NO2 | |
| D. | 向5mL0.1mol/LNaOH溶液中,逐滴加入1mL0.1mol/LAlCl3溶液,边滴加边振荡 |
12.下列物质中,既有离子键又有共价键的是( )
| A. | MgCl2 | B. | Ca(OH)2 | C. | H2O | D. | N2 |
19.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 3mol NF3与水完全反应生成HF、HNO3和NO,转移电子数2NA | |
| B. | 22.4L CO2与过量的Na2O2反应,转移的电子数为NA | |
| C. | 60 g SiO2晶体中含有2 NA个Si-O键 | |
| D. | 常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.3NA |
16.用2mol/L的硝酸银溶液10mL,分别与相同体积的下列溶液恰好完全反应,则下列溶液中物质的量浓度最小的是( )
| A. | BaCl2 | B. | MgCl2 | C. | KCl | D. | FeCl3 |
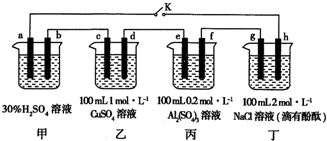
13.下列叙述不正确的是( )
| A. | 与电源正极相连的电极上发生还原反应 | |
| B. | 与电源负极相连的电极称为电解池的阴极 | |
| C. | 电解熔融氯化钠时,阳极上析出Cl2 | |
| D. | 电解是电能转化为化学能的过程 |
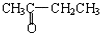 B.
B.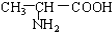 与
与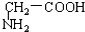
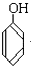 与
与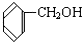 D.CH3CH2C≡CH与CH2═CH-CH═CH2E.
D.CH3CH2C≡CH与CH2═CH-CH═CH2E.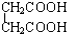 与
与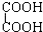 F.戊烯和环丙烯
F.戊烯和环丙烯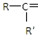 氧化成(R、R′
氧化成(R、R′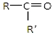 可表示烃基或官能团),若将A中两化合物看作是某单烯烃被臭氧氧化生成的,则该单烯烃的结构简式为CH3CH2CH2CH=C(CH3)CH2CH3.
可表示烃基或官能团),若将A中两化合物看作是某单烯烃被臭氧氧化生成的,则该单烯烃的结构简式为CH3CH2CH2CH=C(CH3)CH2CH3.