题目内容
9.某高分子缓释药物的结构简式见如图: 下列说法不正确的是( )
下列说法不正确的是( )| A. | 该药物在人体胃液中能发生水解反应 | |
| B. | 其水解产物中可能有乙二醇 | |
| C. | 其水解产物中可能有芳香族化合物 | |
| D. | 该高分子化合物通过缩聚反应得到 |
分析 A.该物质中含有酯基,能发生水解反应;
B.该物质水解产物是聚2-甲基丙烯酸、乙二醇、乙酸、邻羟基苯甲酸;
C.邻羟基苯甲酸为芳香族化合物;
D.该高分子化合物是通过碳碳双键加聚反应得到的.
解答 解:A.该物质中含有3个酯基,酯基能发生水解反应,故A正确;
B.该物质水解产物是聚2-甲基丙烯酸、乙二醇、乙酸、邻羟基苯甲酸,所以其水解产物有乙二醇,故B正确;
C.水解生成的邻羟基苯甲酸为芳香族化合物,故C正确;
D.该高分子化合物是通过碳碳双键加聚反应得到的,所以发生的是加聚反应而不是缩聚反应,故D错误;
故选D.
点评 本题考查有机物结构和性质,为高频考点,正确判断该物质中存在的官能团及水解时断键方式是解本题关键,易错选项是B,注意水解产物成分,题目难度不大.

练习册系列答案
相关题目
9.在沸腾炉中进行反应时,被氧化的元素是( )
| A. | 只有硫 | B. | 只有铁 | C. | 硫和铁 | D. | 硫和氧 |
20.A-H及X均为中学化学常见物质,X是一种金属单质,A、B是非金属单质且A在常温下为气体.甲是短周期元素形成的盐,且是某种消毒液的有效成分.它们在一定条件下有如下转化关系(图中条件均已略去).
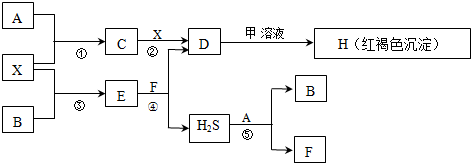
试回答下列问题:
(1)鉴定D中阳离子(不考虑H+)的操作和现象是向少量D溶液中滴入几滴KSCN溶液,无现象,再加入H2O2溶液,溶液显红色.说明D中有Fe2+离子
(2)A与B在一定条件下反应生成一种原子个数比为1:1的分子Y,Y分子中各原子皆达8电子结构,则Y的电子式为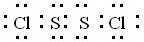 .
.
(3)甲能使D迅速转化为H,甲是NaClO(写化学式),此时甲溶液表现的性质是
氧化性和碱性.将甲溶液与溶液C混合,也能迅速生成H,写出反应的离子方程式Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO.
(4)反应⑤的化学方程式为H2S+Cl2=S↓+2HCl.
(5)25℃,在0.10mol•L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液部分pH与c(S2-)关系如下表(忽略溶液体积的变化、H2S的挥发).
①pH=13时,溶液中的c(H2S)+c(HS-)=0.043mol•L-1.
②某溶液含0.020mol•L-1 Mn2+、0.10mol•L-1 H2S,当溶液pH=5时,Mn2+开始沉淀.[已知:Ksp(MnS)=2.8×10-13].

试回答下列问题:
(1)鉴定D中阳离子(不考虑H+)的操作和现象是向少量D溶液中滴入几滴KSCN溶液,无现象,再加入H2O2溶液,溶液显红色.说明D中有Fe2+离子
(2)A与B在一定条件下反应生成一种原子个数比为1:1的分子Y,Y分子中各原子皆达8电子结构,则Y的电子式为
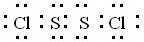 .
.(3)甲能使D迅速转化为H,甲是NaClO(写化学式),此时甲溶液表现的性质是
氧化性和碱性.将甲溶液与溶液C混合,也能迅速生成H,写出反应的离子方程式Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO.
(4)反应⑤的化学方程式为H2S+Cl2=S↓+2HCl.
(5)25℃,在0.10mol•L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液部分pH与c(S2-)关系如下表(忽略溶液体积的变化、H2S的挥发).
| pH | 1 | 3 | 5 | 7 | 9 | 11 | 13 |
| c(S2-) | 1.4×10-19 | 1.4×10-15 | 1.4×10-11 | 6.7×10-7 | 1.9×10-5 | 1.3×10-3 | 5.7×10-2 |
②某溶液含0.020mol•L-1 Mn2+、0.10mol•L-1 H2S,当溶液pH=5时,Mn2+开始沉淀.[已知:Ksp(MnS)=2.8×10-13].
17.有两种气态烃的混合物,将该混合物2.24L(标准状况)完全燃烧,产物先后通过盛浓硫酸洗气瓶和碱石灰的干燥管(假设吸收完全),洗气瓶和干燥管的质量分别增加4.5g和13.2g.则该混合气体的组成和比例可能是( )
| A. | C2H4和C4H6 1:1 | B. | CH4和C4H10 5:1 | ||
| C. | C3H4和C3H8 3:1 | D. | C2H2和C4H8 任意比 |
4.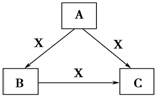 A、B、C、X均为中学化学常见物质,一定条件下有如图所示转化关系(其他产物已略去),下列说法错误的是( )
A、B、C、X均为中学化学常见物质,一定条件下有如图所示转化关系(其他产物已略去),下列说法错误的是( )
 A、B、C、X均为中学化学常见物质,一定条件下有如图所示转化关系(其他产物已略去),下列说法错误的是( )
A、B、C、X均为中学化学常见物质,一定条件下有如图所示转化关系(其他产物已略去),下列说法错误的是( )| A. | 若A、B、C均为焰色反应呈黄色的化合物,则X可为CO2 | |
| B. | 若X为KOH溶液,则A可为AlCl3 | |
| C. | 若X为O2,则A可为硫化氢 | |
| D. | 若X为Cl2,则C可为FeCl3 |
1.苯环实际上不具有碳碳单键和双键的简单交替结构,可以作为证据的事实有( )
①苯的间位二元取代物只有一种;
②苯能在加热和催化剂存在的条件下与氢气加成生成环己烷;
③苯分子中碳碳键的键长均相等(键长是指在分子中两个成键的原子的核间距离);
④苯不能使酸性KMnO4溶液褪色;
⑤苯的邻位二元取代物只有一种;
⑥苯在FeBr3存在的条件下同液溴发生取代反应.
①苯的间位二元取代物只有一种;
②苯能在加热和催化剂存在的条件下与氢气加成生成环己烷;
③苯分子中碳碳键的键长均相等(键长是指在分子中两个成键的原子的核间距离);
④苯不能使酸性KMnO4溶液褪色;
⑤苯的邻位二元取代物只有一种;
⑥苯在FeBr3存在的条件下同液溴发生取代反应.
| A. | ①②③④ | B. | ③④⑤⑥ | C. | ②③④⑥ | D. | 全部 |
18.下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是( )
| A. | NaAlO2和HNO3 | B. | AlCl3和KOH | C. | KHSO4和Ba(OH)2 | D. | K2CO3和HCl |