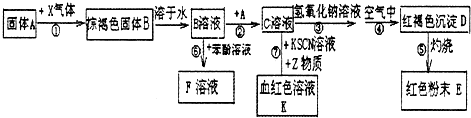
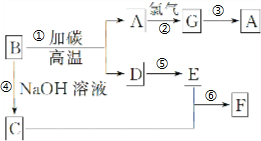
题目内容
苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色.若榨汁时加入维生素C,可有效防止这种现象发生.这说明维生素C具有( )
| A、酸性 | B、碱性 |
| C、较强氧化性 | D、较强还原性 |
考点:人体必需的维生素的主要来源及其摄入途径
专题:有机化学基础
分析:苹果汁由淡绿色变为棕黄色是由于Fe2+被氧化为Fe3+,在这种苹果汁中加入维生素C,可避免该现象,说明维生素C可将Fe3+还原为Fe2+,维生素C具有还原性.
解答:
解:在空气中,氧气能够把+2价铁氧化成+3价;而加入维生素C则能防止这种氧化,说明被氧化的是维生素C而不再是+2价铁,说明维生素C具有还原性,
故选D.
故选D.
点评:本题考查氧化还原反应,难度不大,明确铁元素的化合价变化是解答的关键,应理解氧化反应概念来解答.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
下列有关实验原理或操作,正确的是( )
| A、镀层未破损的镀锌铁和镀层破损后的镀锌铁分别与盐酸反应时产生H2的速度相同 |
| B、用50mL酸式滴定管可准确量取25.00mL的Na2CO3溶液 |
| C、往新配制的淀粉溶液中滴加碘水,溶液显蓝色,加入足量NaOH后溶液褪色 |
| D、配制稀H2SO4溶液时,先在量筒中加入一定体积的水,再在不断搅拌下慢慢加浓H2SO4 |
含有C=C的有机物与O3作用形成不稳定的臭氧化物,臭氧化物在还原剂存在下,与水作用分解为羰基化合物,总反应为:
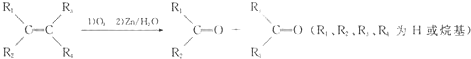
一以下四种物质发生上述反应,所得产物为纯净物且能发生银镜反应的是( )

一以下四种物质发生上述反应,所得产物为纯净物且能发生银镜反应的是( )
| A、(CH3)2═C(CH3)2 |
| B、2-氯-2-丁烯 |
C、 |
D、 |
常温下,0.1mol/LHA溶液的pH>1,0.1mol/LBaOH溶液中c(OH-):c(H+)=1012,将这两种溶液等体积混合,以下离子浓度关系判断正确的是( )
| A、c(H+)<c(OH-)<c(A-)<c(B+) |
| B、c(OH-)<c(H+)<c(B+)<c(A-) |
| C、c(A-)=c(B+)>c(H+)=c(OH-) |
| D、c(A-)=c(B+)<c(H+)=c(OH-) |