题目内容
下列有关实验原理或操作,正确的是( )
| A、镀层未破损的镀锌铁和镀层破损后的镀锌铁分别与盐酸反应时产生H2的速度相同 |
| B、用50mL酸式滴定管可准确量取25.00mL的Na2CO3溶液 |
| C、往新配制的淀粉溶液中滴加碘水,溶液显蓝色,加入足量NaOH后溶液褪色 |
| D、配制稀H2SO4溶液时,先在量筒中加入一定体积的水,再在不断搅拌下慢慢加浓H2SO4 |
考点:化学实验方案的评价
专题:
分析:A.原电池能加快化学反应速率;
B.酸式滴定管可精确到0.01,用来盛放酸性溶液或强氧化性溶液;
C.碘遇淀粉变蓝色,碘单质可与氢氧化钠溶液反应;
D.量筒不能用来配置溶液.
B.酸式滴定管可精确到0.01,用来盛放酸性溶液或强氧化性溶液;
C.碘遇淀粉变蓝色,碘单质可与氢氧化钠溶液反应;
D.量筒不能用来配置溶液.
解答:
解:A.破损后锌铁与盐酸形成原电池,原电池能加快化学反应速率,故A错误;
B.Na2CO3溶液呈碱性,应用碱式滴定管,故B错误;
C.碘遇淀粉变蓝色,碘单质可与氢氧化钠溶液反应生成碘化钠和碘酸钠而褪色,故C正确;
D.量筒不能用来配置溶液,应用烧杯,故D错误.
故选C.
B.Na2CO3溶液呈碱性,应用碱式滴定管,故B错误;
C.碘遇淀粉变蓝色,碘单质可与氢氧化钠溶液反应生成碘化钠和碘酸钠而褪色,故C正确;
D.量筒不能用来配置溶液,应用烧杯,故D错误.
故选C.
点评:本题考查碘单质的性质、原电池原理、实验操作等知识,难度不大,注意锌与铁在酸溶液中能构成原电池.

练习册系列答案
相关题目
在一定温度下,苯和苯甲酸的气体混合物VL,完全燃烧生成CO2和H2O,消耗相同状态下的O27.5VL,则混合气体中苯和苯甲酸的体积比为( )
| A、1:1 | B、2:1 |
| C、1:2 | D、任意比 |
下列各组物质混合后,最终有氢氧化钠生成的选项是( )
①Na与足量CuSO4 的溶液; ②Ca(OH)2 溶液与Na2CO3 溶液;
③Ca(OH)2 溶液和足量的NaCl 溶液; ④Na2O2与足量FeCl2 的溶液;
⑤Na与足量Na2SO4 的溶液; ⑥Na2O2与足量MgCl2 溶液;
⑦Na2O与足量NaHCO3 溶液; ⑧Na与足量Na2CO3 溶液.
①Na与足量CuSO4 的溶液; ②Ca(OH)2 溶液与Na2CO3 溶液;
③Ca(OH)2 溶液和足量的NaCl 溶液; ④Na2O2与足量FeCl2 的溶液;
⑤Na与足量Na2SO4 的溶液; ⑥Na2O2与足量MgCl2 溶液;
⑦Na2O与足量NaHCO3 溶液; ⑧Na与足量Na2CO3 溶液.
| A、①③⑧ | B、②⑤⑧ |
| C、④⑤⑧ | D、③⑥⑦ |
苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为棕黄色.若榨汁时加入维生素C,可有效防止这种现象发生.这说明维生素C具有( )
| A、酸性 | B、碱性 |
| C、较强氧化性 | D、较强还原性 |
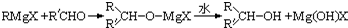
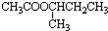 的过程如下(反应条件没有列出):
的过程如下(反应条件没有列出):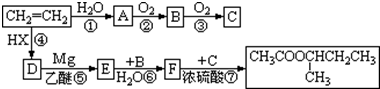
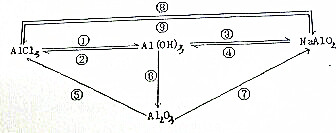
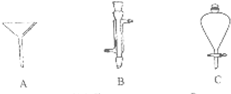 Ⅰ、如图是几种实验中常用的仪器:写出序号所代表的仪器的名称:
Ⅰ、如图是几种实验中常用的仪器:写出序号所代表的仪器的名称:
