题目内容
下列说法中正确的是( )
| A、增大反应物浓度,能增大活化分子百分数,所以反应速率增大 |
| B、使用正催化剂,能增大活化分子百分数,所以反应速率增大 |
| C、对于任何反应,增大压强都可加快反应速率 |
| D、升高温度,只能增大吸热反应的反应速率 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:升高温度、增大压强,反应速率都增大,压强、浓度只影响单位体积活化分子的数目,温度、催化剂影响活化分子的百分数,以此解答该题.
解答:
解:A.增大反应物浓度,单位体积活化分子数目增大,但活化分子百分数不变,故A错误;
B.催化剂可以降低反应的活化能,增大活化分子百分数,故B正确;
C.压强只影响气体的反应速率,故C错误;
D.升高温度,无论是吸热反应还是放热反应,反应速率都增大,故D错误.
故选B.
B.催化剂可以降低反应的活化能,增大活化分子百分数,故B正确;
C.压强只影响气体的反应速率,故C错误;
D.升高温度,无论是吸热反应还是放热反应,反应速率都增大,故D错误.
故选B.
点评:本题考查活化能及其对反应速率的影响,题目难度不大,注意温度、浓度、压强、催化剂等外界条件对化学反应速率的影响的根本原因是对活化分子的影响,但影响原因不同.

练习册系列答案
相关题目
某温度下,将3mol A和2mol B充入一密闭容器中,发生下列反应:aA(气)+B(气)?C(气)+D(气),5分钟后达到平衡状态,已知一定温度下,各物质的平衡浓度符合下列关系:[A]a[B]=[C][D],若在温度不变的条件下,将上述容器的体积扩大为原来的10倍,发现A的转化率不发生变化,则B的转化率为( )
| A、60% | B、40% |
| C、24% | D、4% |
向27.2gCu、CuO、Cu2O的混合物中加入某浓度的稀硝酸0.5L,生成NO和Cu(NO3)2.在所得溶液中加入1.0mol/L的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g,下列说法不正确的是( )
| A、原混合物中Cu和O的物质的量之比为2:1 |
| B、硝酸的物质的量浓度为2.6mol/L |
| C、产生的NO在标准状况下的体积为4.48L |
| D、Cu、CuO、Cu2O与硝酸反应后剩余HNO3为0.2mol |
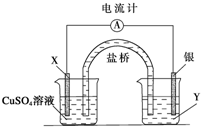 根据下列氧化还原反应2FeCl3+Cu═2FeCl2+CuCl2设计一个原电池:
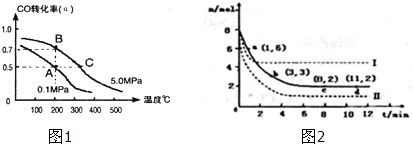
根据下列氧化还原反应2FeCl3+Cu═2FeCl2+CuCl2设计一个原电池: 汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.某研究小组在实验室以Ag-ZSM-5 为催化剂,测得NO转化为N2的转化率随温度变化情况如图.
汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题.某研究小组在实验室以Ag-ZSM-5 为催化剂,测得NO转化为N2的转化率随温度变化情况如图.