题目内容
下列分散系属于胶体的是( )
| A、石灰水 | B、豆浆 |
| C、泥水 | D、蔗糖水 |
考点:分散系、胶体与溶液的概念及关系
专题:溶液和胶体专题
分析:分散系的根本区别在于分散质微粒直径的大小,小于100nm为溶液,大于100nm为浊液,在1nm~100nm的为胶体.
解答:
解:石灰水和蔗糖水分散质微粒直径小于1nm是溶液;泥水分散质微粒直径大于100nm,属于悬浊液;豆浆分散质微粒直径的大小在1nm~100nm之间,属于胶体.
故选B.
故选B.
点评:本题考查胶体的特点,明确胶体分散质微粒直径在1~100nm之间是解答的关键,是对基础内容的考查,题目较简单.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
可逆反应A(g)+3B(g)?2C(g);△H=-QkJ/mol.有甲、乙两个容积相同且固定不变的密闭容器,向甲容器中加入1mol A和3mol B,在一定条件下达到平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2mol C达到平衡后吸收热量为Q2 kJ,已知Q1=2Q2.下列叙述正确的是( )
| A、甲中A的转化率为75% | ||||
| B、Q1+Q2<Q | ||||
C、达到平衡后,再向乙中加入
| ||||
| D、乙中热化学方程式为2C(g)?A(g)+3B(g);△H=+Q2 kJ/mol |
1,8-二硝基萘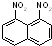 苯环上的二溴代物与四溴代物的种类分别有( )
苯环上的二溴代物与四溴代物的种类分别有( )
 苯环上的二溴代物与四溴代物的种类分别有( )
苯环上的二溴代物与四溴代物的种类分别有( )| A、9种、9种 |
| B、9种、15种 |
| C、15种、9种 |
| D、15种、15种 |
一个氖原子的质量是a g,一个12C原子的质量为b g,NA表示阿伏德罗常数,下列说法不正确的是( )
A、该氖原子的相对原子质量是
| ||
| B、氖原子的摩尔质量为a?NA g/mol | ||
C、Wg该氖原子的物质的量为
| ||
D、Wg该氖原子所含原子数为
|
下列有关热化学方程式的叙述正确的是( )
| A、已知CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-893.0kJ/mol,则甲烷的燃烧热为893.0kJ?mol-1 | ||
| B、已知4P(红磷,s)═P4(白磷,s);△H>0,则白磷比红磷稳定 | ||
C、含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,反应的化学方程式为:NaOH(aq)+
| ||
D、己知C(s)+O2(g)═CO2(g);△H1C(s)+
|
下列现象或事实可用同一原理解释的是( )
| A、MnO2与氯酸钾制氧气和MnO2与浓盐酸制氯气 |
| B、蛋白质溶液中加入硫酸钠浓溶液或硫酸铜溶液时均生成沉淀 |
| C、乙烯和NaOH溶液都能使溴水退色 |
| D、镀锌铁和镀锡铁在镀层被破坏后铁的腐蚀情况不同 |
下列热化学方程式或离子方程式中,正确的是( )
| A、甲烷的燃烧热为890.3 kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ?mol-1 | ||||||||
| B、500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中完全反应生成NH3(g),放热19.3 kJ,其热化学方程式为: N2(g)+3H2(g)
| ||||||||
| C、氯化镁溶液与氨水反应:Mg 2++2OH -=Mg(OH)2↓ | ||||||||
D、已知强酸与强碱的稀溶液反应的中和热为57.3 KJ/mol,则0.1mol醋酸与0.1mol氢氧化钠的稀溶液反应的热化学方程式为:
|
下列离子方程式书写正确的是( )
| A、硫酸铜溶液与氢氧化钡溶液反应Ba2++SO42-═BaSO4↓ |
| B、氢氧化铝治疗胃酸 Al(OH)3+3H+═Al3++3H2O |
| C、铜与硝酸银溶液反应 Cu+Ag+═Cu2++Ag |
| D、硫酸氢钠溶液与氢氧化钠溶液反应OH-+H+═H2O |
对于达到平衡的可逆反应H2(g)+I2(g)?2HI(g) (正反应是放热反应),欲使混合气体的颜色变深,应采取的措施是( )
| A、升高温度 | B、降低温度 |
| C、增大压强 | D、减少压强 |