题目内容
下列有关热化学方程式的叙述正确的是( )
| A、已知CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-893.0kJ/mol,则甲烷的燃烧热为893.0kJ?mol-1 | ||
| B、已知4P(红磷,s)═P4(白磷,s);△H>0,则白磷比红磷稳定 | ||
C、含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,反应的化学方程式为:NaOH(aq)+
| ||
D、己知C(s)+O2(g)═CO2(g);△H1C(s)+
|
考点:热化学方程式
专题:化学反应中的能量变化
分析:A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,选项中水是气体不是稳定氧化物;
B、物质能量越高越活泼;
C、结合中和热概念分析,含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,40g氢氧化钠完全反应放热57.4KJ;
D、一氧化碳生成二氧化碳放热,焓变为负值比较大小;
B、物质能量越高越活泼;
C、结合中和热概念分析,含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,40g氢氧化钠完全反应放热57.4KJ;
D、一氧化碳生成二氧化碳放热,焓变为负值比较大小;
解答:
解:A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,选项中水是气体不是稳定氧化物,不符合燃烧热概念,故A错误;
B、物质能量越高越活泼,4P(红磷,s)═P4(白磷,s);△H>0,则白磷能量比红磷高,红磷比白磷稳定,故B错误;
C、结合中和热概念分析,含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,40g氢氧化钠完全反应放热57.4KJ,NaOH(aq)+
H2SO4(aq)═Na2SO4(aq)+H2O(l);△H=-57.4kJ?mol-1符合中和热概念,故C正确;
D、一氧化碳生成二氧化碳放热,焓变为负值比较大小,C(s)+O2(g)═CO2(g);△H1 C(s)+
O2(g)═CO(g);△H2,则△H1<△H2,故D错误;
故选C.
B、物质能量越高越活泼,4P(红磷,s)═P4(白磷,s);△H>0,则白磷能量比红磷高,红磷比白磷稳定,故B错误;
C、结合中和热概念分析,含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,40g氢氧化钠完全反应放热57.4KJ,NaOH(aq)+
| 1 |
| 2 |
D、一氧化碳生成二氧化碳放热,焓变为负值比较大小,C(s)+O2(g)═CO2(g);△H1 C(s)+
| 1 |
| 2 |
故选C.
点评:本题考查了燃烧热、中和热概念分析判断,热化学方程式书写,焓变大小比较注意放热反应的焓变为负值,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
化学与生产、生活、社会密切相关,下列说法正确的是( )
| A、煤经气化和液化两个物理过程后可变为清洁能源,这是煤综合利用的主要方法 |
| B、蛋白质、淀粉、纤维素、油脂等都能在人体内水解并提供能量 |
| C、利用风能发电、使用太阳能热水器、应用无氟制冷剂均有利于降低大气中的二氧化碳 |
| D、塑料袋在全球“失宠”,有偿使用成为风尚,是因为塑料袋填埋占用土地,且难以降解,会造成“白色污染” |
下列实验装置、试剂选用或操作正确的是( )
A、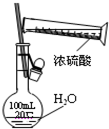 配制一定浓度的稀硫酸 |
B、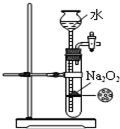 实验室制备氧气 |
C、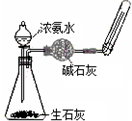 实验室制备氨气 |
D、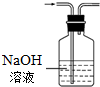 除去CO2中的HCl |
 下列叙述正确的是( )
下列叙述正确的是( )| A、为提醒人们在使用浓H2SO4时要注意安全,贮存浓H2SO4的容器上贴有右图标识 |
| B、实验室可通过蒸馏的方法除去自来水中含有的Cl-等杂质制蒸馏水 |
| C、做焰色反应实验时,应先将铂丝(或铁丝)用稀硫酸洗净后,在酒精灯外焰上灼烧至没有颜色时,再蘸取待检溶液进行实验 |
| D、由于碱金属单质化学性质活泼,实验室中的各种碱金属单质均保存在煤油中 |
X、Y、Z、W是前20号元素中的4种元素,分布在三个周期,原子序数依次增大,它们可以组成某矿物质:WYZX,四种元素中W,Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,W能与冷水剧烈反应,Y,Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等,Y、Z位于同周期,Z单质是一种良好的半导体.下列说法不正确的是( )
| A、原子半径:W>Y>Z>X |
| B、气态氢化物的稳定性:X>Z |
| C、金属性:Y<W |
| D、Y、Z的氧化物都能和酸或碱反应,都是两性氧化物 |
下列分散系属于胶体的是( )
| A、石灰水 | B、豆浆 |
| C、泥水 | D、蔗糖水 |
下列物质中,属于碱的是( )
| A、纯碱 | B、烧碱 |
| C、生石灰 | D、碱式碳酸铜 |
祖母绿是含铬(以Cr2O3形式存在)等微量元素的矿物,其主要成分为Be3Al2Si6O18(Be3Al2Si6O18为无色透明),下列说法不正确的是( )
| A、祖母绿是一种硅酸盐矿物 |
| B、其主要成分可用氧化物形式表示:3BeO?Al2O3?6SiO2 |
| C、绿色是Cr2O3表现出来的 |
| D、祖母绿是多种氧化物组成的混合物 |
一定条件下,在密闭容器内,SO2氧化成SO3的热化学方程式为:2SO2(g)+O2(g)?2SO3(g);
△H=-a kJ?mol-1在相同条件下,要想得到2akJ热量,加入各物质的物质的量可能是( )
△H=-a kJ?mol-1在相同条件下,要想得到2akJ热量,加入各物质的物质的量可能是( )
| A、4molSO2和2molO2 |
| B、5molSO2和3molO2 |
| C、4molSO2和4molO2 |
| D、2molSO2、1molO2和2molSO3 |