题目内容
4.下表为元素周期表的一部分,请参照元素①-⑩在表中的位置,用化学用语回答下列问题:| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①、③、⑤的最高价最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式).
(3)②、③、④三种元素可形成的离子,离子半径由大到小的顺序为K+>Ca2+>Mg2+(填离子符号).
(4)①和⑨两元素形成化合物的化学式为NaBr,该化合物灼烧时的焰色为
黄色;该化合物的溶液与元素⑧的单质反应的离子方程式为Cl2+2Br-=2Cl-+Br2
(5)用电子式表示第三周期元素中金属性最强的元素和非金属性最强的元素形成化合物的过程
 .
.
分析 根据元素在周期表中位置知,①②③④⑤⑥⑦⑧⑨⑩分别是Na、K、Mg、Ca、Al、C、F、Cl、Br、Ar元素,
(1)稀有气体元素最不活泼;同一周期中,元素的金属性随着原子序数的增大而减弱,同一主族中,元素的金属性随着原子序数的增大而增强;
(2)金属性越强,最高价氧化物对应水合物的碱性越强;
(3)电子层数越多,离子半径越大,电子层结构相同的离子,离子半径随着原子序数的增大而减小;
(4)钠与溴结合形成溴化钠;灼烧溴化钠呈现黄色;溴化钠溶液与氯气反应生成氯化钠和溴单质;
(5)第三周期元素中金属性最强的元素为和非金属性最强的元素分别为Na、Cl,二者形成的化合物为NaCl,NaCl为离子化合物,用电子式表示出氯化钠的形成过程.
解答 解:根据元素在周期表中位置知,①②③④⑤⑥⑦⑧⑨⑩分别是Na、K、Mg、Ca、Al、C、F、Cl、Br、Ar元素,
(1)这几种元素中最不活泼的是Ar元素,金属性最强是元素是K,
故答案为:Ar;K;
(2)①、③、⑤分别为Na、Mg、Al,同一周期中,原子序数依次增大,金属性依次减弱,则金属性最强最强的为Na,Na的最高价氧化物对应水合物为NaOH,
故答案为:NaOH;
(3)②、③、④分别为K、Mg、Ca,对应离子分别为钾离子、镁离子、钙离子,镁离子的电子层最少,其离子半径最小,钾离子的核电荷数较小,则钾离子半径最大,所以离子半径大小为:K+>Ca2+>Mg2+,
故答案为:K+>Ca2+>Mg2+;
(4)①和⑨分别为Na、Br,二者形成化合物为NaBr,NaBr中含有钠元素,在灼烧时的焰色为黄色;元素⑧的单质为氯气,溴化钠溶液与氯气反应生成氯化钠和溴,反应的离子方程式为:Cl2+2 Br-=2Cl-+Br2,
故答案为NaBr;黄;Cl2+2 Br-=2Cl-+Br2;
(5)第三周期元素中金属性最强的元素为和非金属性最强的元素分别为Na、Cl,二者形成的化合物为NaCl,NaCl为离子化合物,书写电子式时注意,左边写钠原子和氯原子电子式,右边写氯化钠的电子式,中间用箭头连接,用电子式表示氯化钠的形成过程为: ,
,
故答案为: .
.
点评 本题考查了位置、结构与性质的关系及应用,题目难度中等,涉及离子方程式书写、电子式、离子半径大小比较、元素周期律应用等知识,明确元素周期表结构、元素周期律内容为解答关键,试题培养了学生的分析、理解能力及灵活应用能力.

 计算高手系列答案
计算高手系列答案| A. | 铜片 | B. | 硫酸溶液 | C. | 氯化钠 | D. | 酒精 |
| A. | Na2SO3溶液(BaCl2) | B. | FeCl2溶液(KSCN) | ||
| C. | 海带灰过滤所得的溶液(淀粉溶液) | D. | NaOH溶液(CaCl2) |
| A. | NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3-+OH-+Ba2+═H2O+BaCO3↓ | |
| B. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -═2 Al(OH)3↓+3BaSO4↓ | |
| C. | 向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- | |
| D. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ |
| A. | 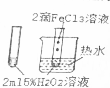 验证FeCl3对H2O2分解反应有催化作用 | |
| B. | 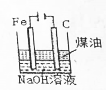 制备Fe(OH)2并能较长时间观察其颜色 | |
| C. |  验证盐酸、碳酸、苯酚酸性的强弱 | |
| D. |  制取乙酸乙酯 |
| A. | 分离、提纯→确定化学式→确定最简式→确定结构式 | |
| B. | 分离、提纯→确定最简式→确定化学式→确定结构式 | |
| C. | 分离、提纯→确定结构式→确定最简式→确定化学式 | |
| D. | 确定化学式→确定最简式→确定结构式→分离、提纯 |
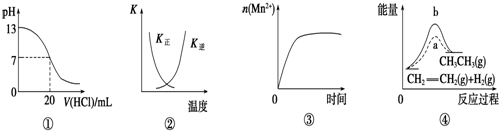
| A. | 图①表示25℃时,用0.1 mol/L盐酸滴定20 mL 0.1 mol/L NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. | 图②中曲线表示反应2SO2(g)+O2(g)?2SO3(g)△H<0正、逆反应的平衡常数K随温度的变化 | |
| C. | 图③表示10 mL 0.01 mol/L KMnO4酸性溶液与过量的0.1 mol/L H2C2O4溶液混合时,n(Mn2+)随时间的变化 | |
| D. | 图④中a、b曲线分别表示反应:CH2═CH2(g)+H2(g)→CH3CH3(g)△H<0使用和未使用催化剂时,反应过程中的总能量变化 |
| A. | 标准状况下,1L庚烷完全燃烧后,所生成的气态产物的分子数为$\frac{7}{22.4}$NA | |
| B. | 100ml 0.1mol/LCH3COOH溶液跟足量锌反应,生成的氢气分子数为0.01NA | |
| C. | 0.1mol CH4所含质子数为NA | |
| D. | 0.5mol C2H4中含有的C=C双键数为NA |
