题目内容
写出下列各烷烃的分子式.
(1)同温同压下蒸气的密度是H2的36倍的烷烃 .
(2)分子中含有200个氢原子的烷烃 .
(3)1L烷烃的蒸气完全燃烧时,生成同温同压下的水蒸气15L .
(4)分子中含有22个共价键的烷烃 .
(1)同温同压下蒸气的密度是H2的36倍的烷烃
(2)分子中含有200个氢原子的烷烃
(3)1L烷烃的蒸气完全燃烧时,生成同温同压下的水蒸气15L
(4)分子中含有22个共价键的烷烃
考点:有关有机物分子式确定的计算
专题:有机物分子组成通式的应用规律
分析:(1)根据密度之比等于摩尔质量之比进行计算;
(2)根据烷烃的通式CnH(2n+2)和B的分子中含有200个氢原子计算;
(3)根据同温同压下,体积比等于物质的量之比,再根据氢原子守恒计算出n;
(4)烷烃的组成为CnH2n+2,含有的共价键数目为3n+1,据此分析.
(2)根据烷烃的通式CnH(2n+2)和B的分子中含有200个氢原子计算;
(3)根据同温同压下,体积比等于物质的量之比,再根据氢原子守恒计算出n;
(4)烷烃的组成为CnH2n+2,含有的共价键数目为3n+1,据此分析.
解答:
解:烷烃的通式为:CnH(2n+2),烷烃的相对分子量为:14n+2,
(1)密度之比等于摩尔质量之比,就等于相等分子量之比,该有机物的相对分子质量为:36×2=72=14n+2,解得n=5,所以分子式为C5H12,故答案为:C5H12;
(2)烷烃的分子中含有200个氢原子,即2n+2=200,解得:n=99,所以分子式为C99H200,故答案为:C99H200;
(3)1L烷烃的蒸气完全燃烧时,生成同温、同压下15L水蒸气,根据氢原子守恒,所以烷烃分子中含30个氢原子,即2n+2=30,n=14,所以的分子式为C14H30,故答案为:C14H30;
(4)烷烃的组成为CnH2n+2,含有的共价键数目为3n+1,该烷烃有22个共价键,则:3n+1=22,解得n=7,所以该烷烃中碳原子数目为7,分子式为C7H16,故答案为:C7H16.
(1)密度之比等于摩尔质量之比,就等于相等分子量之比,该有机物的相对分子质量为:36×2=72=14n+2,解得n=5,所以分子式为C5H12,故答案为:C5H12;
(2)烷烃的分子中含有200个氢原子,即2n+2=200,解得:n=99,所以分子式为C99H200,故答案为:C99H200;
(3)1L烷烃的蒸气完全燃烧时,生成同温、同压下15L水蒸气,根据氢原子守恒,所以烷烃分子中含30个氢原子,即2n+2=30,n=14,所以的分子式为C14H30,故答案为:C14H30;
(4)烷烃的组成为CnH2n+2,含有的共价键数目为3n+1,该烷烃有22个共价键,则:3n+1=22,解得n=7,所以该烷烃中碳原子数目为7,分子式为C7H16,故答案为:C7H16.
点评:本题考查了有机物烷烃分子式的确定,题目难度中等,要求学生掌握物质的量与摩尔质量转化关系、同温同压下气体的摩尔质量与密度关系,并且能够学会用通式表示烷烃的燃烧反应.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
下列关于氢键说法正确的是( )
| A、H2S比H2O的沸点低的原因是H2O分子间存在氢键 |
| B、氯化氢极易溶于水是因为氯化氢溶于水时形成了氢键 |
| C、氨易液化与氨分子间存在氢键无关 |
| D、H2O是一种非常稳定的化合物,这是由于氢键所致 |
下列说法正确的是( )
①在水中氢、氧原子间均以化学键相结合;
②金属和非金属化合时一定形成离子键;
③离子键是阳离子、阴离子的相互吸引作用;
④根据电离方程式:HCl═H++Cl-,可判断HCl分子里存在离子键;
⑤H2和Cl2 的反应过程是H2 、Cl2 分子中共价键发生断裂生成H、Cl原子,而后原子形成离子键的过程.
①在水中氢、氧原子间均以化学键相结合;
②金属和非金属化合时一定形成离子键;
③离子键是阳离子、阴离子的相互吸引作用;
④根据电离方程式:HCl═H++Cl-,可判断HCl分子里存在离子键;
⑤H2和Cl2 的反应过程是H2 、Cl2 分子中共价键发生断裂生成H、Cl原子,而后原子形成离子键的过程.
| A、①②⑤ | B、都不正确 |
| C、④ | D、②③④⑤ |
 在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.下列叙述错误的是(已知NH4++OH-═NH3?H2O)( )
在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入4mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.下列叙述错误的是(已知NH4++OH-═NH3?H2O)( )| A、原溶液中n(Mg2+):n(Al3+)=5:1 |
| B、原溶液的c(H+)=0.8mol?L-1 |
| C、x与y的差值为0.01mol |
| D、原溶液中c(Cl-)=1.32mol?L-1 |
设NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA |
| B、50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
| C、常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了28g,则转移的电子数为2NA |
| D、含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol?L-1 |
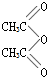 ,
, +AS
+AS +CH3COOH
+CH3COOH



