题目内容
7.下列离子方程式正确的是( )| A. | 将过量SO2通入稀氨水中:SO2+NH3•H2O═HSO3-+NH4+ | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 大理石溶于醋酸中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O═[Al(OH)4]-+4NH4+ |
分析 A.反应生成亚硫酸氢铵;
B.发生氧化还原反应生成碘化亚铁、碘、水;
C.醋酸在离子反应中保留化学式;
D.反应生成氢氧化铝和氯化铵.
解答 解:A.将过量SO2通入稀氨水中的离子反应为SO2+NH3•H2O═HSO3-+NH4+,故A正确;
B.Fe(OH)3溶于氢碘酸的离子反应为2I-+2Fe(OH)3+6H+═2Fe2++6H2O+I2,故B错误;
C.大理石溶于醋酸中的离子反应为CaCO3+2CH3COOH═2CH3COO-+Ca2++H2O+CO2↑,故C错误;
D.AlCl3溶液中加入过量稀氨水的离子反应为Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故D错误;
故选A.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
18.下列物质间的转化过程,属于氧化反应的是( )
| A. | Mg→MgO | B. | CaO→CaCO3 | C. | Cl2→NaCl | D. | H2SO4→SO2 |
2.20℃、1大气压下,lgH2完全燃烧生成稳定的氧化物,测得放出142.9kJ的热量.下列表示该反应的热化学方程式正确的是( )
| A. | 2H2(g)+O2(g)═2H2O(1)△H=-149.2 kJ/mol | B. | H2(g)+O2(g)═H2O(1)△H=+285.8 kJ/mol | ||
| C. | 2H2(g)+O2(g)═2H2O(g)△H=-571.6kJ/mol | D. | 2H2(g)+O2(g)═2H2O(1)△H=-571.6kJ/mol |
19.在密闭容器中A与B反应生成C,已知:2v(B)=3v(A),3v(C)=2v(B).则此反应为( )
| A. | A+3B=2C | B. | 3A+B=2C | C. | A+B=C | D. | 2A+3B=2C |
16.在pH=1的溶液中,下列各组离子因氧化还原反应而不能大量共存的是( )
| A. | S2-、Na+、SO42-、K+ | B. | K+、SO32-、Na+、S2- | ||
| C. | NH4+、Na+、NO3-、Cl- | D. | SO42-、NH4+、Na+、HCO3- |





 ;
;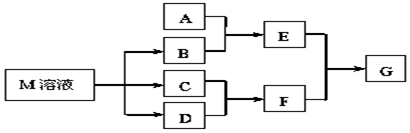

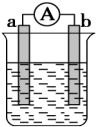 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题: