题目内容
11.实验室需用480毫升0.1mol•L-1的硫酸铜溶液,若用胆矾(CuSO4•5H2O)或无水硫酸铜配制,下列操作中正确的是( )| A. | 取12.0 g胆矾溶于480m L水中 | |
| B. | 取8.0 g CuSO4溶于480m L水 | |
| C. | 取12.5 g胆矾溶于水,再转入500mL容量瓶中,加水至刻度 | |
| D. | 取12.5 g胆矾加热除去结晶水,再放入500mL容量瓶中,加水至刻度 |
分析 实验室没有480mL的容量瓶,应选择大于480mL且规格相近的容量瓶,故应选择500mL容量瓶.配制溶液的体积为500mL,根据n=cV计算硫酸铜的物质的量,需要硫酸铜物质的量等于硫酸铜晶体的物质的量,再根据m=cVM计算所需硫酸铜的质量或硫酸铜晶体的质量,据此判断.注意500mL是溶液的体积,不是溶剂的体积.
解答 解:由于实验室没有480mL的容量瓶,只能选用500mL容量瓶,配制500mL 0.1mol/L的硫酸铜溶液,需要硫酸铜的物质的量为:0.1mol/L×0.5L=0.05mol,硫酸铜的质量为:160g/mol×0.05mol=8.0g,需要胆矾质量为:250g/mol×0.05mol=12.5g,
A.应选用500 mL容量瓶,配制500mL溶液,故A错误;
B.应选用500 mL容量瓶,配制500mL溶液,故B错误;
C.应选用500 mL容量瓶,配制500mL溶液,需要称取12.5g胆矾,故C正确;
D.不能再容量瓶中溶解胆矾,故D错误;
故选C.
点评 本题考查一定物质的量浓度溶液的配制,比较基础,根据c=$\frac{n}{V}$理解溶液的配制、物质的量浓,注意一定容量规格的容量瓶只能配制相应体积的溶液.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
1.有一电化学装置如图所示,其中a、b、c、d均为石墨电极. 则下列有关说法正确的是( )
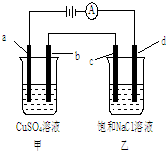

| A. | 甲烧杯中溶液的pH增大,乙烧杯中溶液的pH减小 | |
| B. | 电解一段时间后,b极质量增加,d极附近滴加酚酞溶液变红 | |
| C. | 甲烧杯中a电极发生氧化反应,电极反应式为:4OH-+4e-═O2↑+2H2O | |
| D. | C是阳极,电子从d电极通过溶液流向c电极 |
2.下列反应中,不属于氧化还原反应的是( )
| A. | 2Na+2H2O=2NaOH+H2↑ | B. | 3NO2+H2O=2HNO3+NO | ||
| C. | 2Al+2NaOH+6H2O=2NaAlO2+3H2↑ | D. | CaCO3=CaO+CO2↑ |
19.下列实验操作都能够达到预期目的是( )
①用pH试纸测得某溶液pH为3.5
②用米汤直接检验食用盐中是否含有碘元素
③用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
④滴入酚酞溶液确定纯碱中有无烧碱
⑤用酸式滴定管量取20.00mL高锰酸钾酸性溶液
⑥蒸干AlCl3溶液可得纯净的无水氯化铝.
①用pH试纸测得某溶液pH为3.5
②用米汤直接检验食用盐中是否含有碘元素
③用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
④滴入酚酞溶液确定纯碱中有无烧碱
⑤用酸式滴定管量取20.00mL高锰酸钾酸性溶液
⑥蒸干AlCl3溶液可得纯净的无水氯化铝.
| A. | ②④⑥ | B. | ②⑥ | C. | ⑤ | D. | ④⑤⑥ |
6.下列各组溶液,不用其他任何试剂或试纸无法鉴别的是( )
| A. | 稀硫酸和碳酸钠溶液 | B. | 氯化铝溶液和氢氧化钠溶液 | ||
| C. | 稀盐酸和偏铝酸钠溶液 | D. | 碳酸钠溶液和氯化钠溶液 |
16.下列有关物质分类和氧化还原的描述正确的是( )
| A. | 酸性氧化物一定是非金属氧化物,混合物、分散系、胶体有从属关系 | |
| B. | 元素的单质可由氧化或还原含该元素的化合物来制得 | |
| C. | 得电子越多的氧化剂,其氧化性就越强;含最高价元素的化合物一定具有强的氧化性 | |
| D. | 烧碱、熟石灰均属于碱,酸、碱、盐之间发生的反应均属于复分解反应 |
3.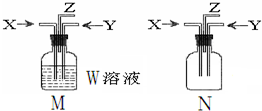 利用如图M、N两个装置进行相关实验,下列有关说法正确的是( )
利用如图M、N两个装置进行相关实验,下列有关说法正确的是( )
 利用如图M、N两个装置进行相关实验,下列有关说法正确的是( )
利用如图M、N两个装置进行相关实验,下列有关说法正确的是( )| 选项 | 所用装置 | 描述 | 结论 |
| A | M | W:BaCl2;X:CO2 Y:SO2 | M中有白色沉淀生成 |
| B | M | W:饱和食盐水;先通入X:CO2,再通入Y:NH3 | M中制得小苏打 |
| C | N | X:NH3 Y:Cl2 | Z出口有白烟产生 |
| D | N | X:NH3Y:O2 | Z出口有红棕色气体 |
| A. | A | B. | B | C. | C | D. | D |
20.常温下,下列有关溶液的pH或微粒的物质的量浓度关系的判断不正确的是( )
| A. | pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,所得溶液的pH<7 | |
| B. | 某物质的溶液中由水电离出的c(H+)=1×10-amol•L-1,若a>7,则该溶液的pH一定为14-a | |
| C. | 将0.2mol•L-1的某一元酸HA溶液和0.1mol•L-1 NaOH溶液等体积混合后,混合溶液的pH大于7,则反应后的混合溶液中:2c(OH-)=2c(H+)+c(HA)-c(A-) | |
| D. | pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合溶液的pH=7,则反应后的混合溶液中:2c(R2-)+c(HR-)=c(Na+) |