题目内容
20.有关物质的转化关系如图所示(部分物质和条件已略去),A是一种淡黄色粉末,B是某种矿物中的主要成分,D、Y是空气含量最多的两种气体,J是一种紫红色金属,X是最常见的无色液体.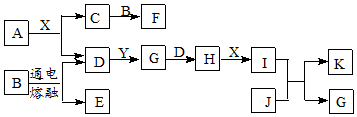
(1)A的化学式为Na2O2
(2)Y的电子式为
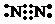
(3)I与J反应的化学方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(4)C与B在溶剂X中反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O.
分析 A是一种淡黄色粉末,B是某种矿物中的主要成分,D、Y是空气含量最多的两种气体,X是最常见的无色液体,结合图中转化可知,X为H2O,A为Na2O2,则D为O2,C为NaOH,B为Al2O3,E为Al,F为NaAlO2,再结合J是一种紫红色金属,可知J为Cu,Y为N2,G为NO,H为NO2,I为HNO3,K为Cu( NO3)2,以此来解答.
解答 解:(1)A的化学式为Na2O2,故答案为:Na2O2;(2)Y的电子式为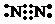
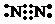
(3)I与J反应的化学方程式为3Cu+8HNO3 (稀)=3Cu( NO3)2+2NO↑+4H2O,故答案为:3Cu+8HNO3 (稀)=3Cu( NO3)2+2NO↑+4H2O; (4)C与B在溶剂X中反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O,故答案为:Al2O3+2OH-=2AlO2-+H2O.
点评 本题考查无机物的推断,为高频考点,把握物质的性质、发生的反应、相互转化为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
10.某溶液只可能含有下列离子中的几种:K+、NH4+、SO42-、AlO2-、NO3-(不考虑水的电离).取200mL该溶液,分为等体积的两份,分别做下列两个实验.实验1:向第一份溶液中加入足量的烧碱并加热,在标准状况下产生的气体体积为224mL.实验2:向第二份溶液中加入足量的BaCl2溶液,生成沉淀2.33g,下列说法正确的是( )
| A. | 该溶液中可能含有K+ | |
| B. | 该溶液中肯定含有NH4+、SO42-、AlO2-、NO3- | |
| C. | 该溶液中一定不含NO3- | |
| D. | 该溶液中一定含K+,且c(K+)≥0.1 mol•L-1 |
15.下列各组两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A. | Cu(OH)2 和盐酸; Cu(OH)2 和 CH3COOH | |
| B. | BaCl2 和 Na2SO4; Ba(OH)2 和 CuSO4 | |
| C. | NaHCO3 和 NaHSO4; Na2CO3 和 NaHSO4 | |
| D. | NaHCO3(过量) 和 Ca(OH)2; Ca(HCO3)2 和 NaOH(过量) |
12.一定条件下,一种反应物过量而另一种反应物仍不能完全反应的是( )
| A. | 氧气和二氧化硫 | B. | 盐酸和锌粒 | C. | 浓硝酸和铜屑 | D. | 醋酸和烧碱 |
9. 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)
(1)该反应的平衡常数表达式K=$\frac{c(C{H}_{3}OH)}{c(CO)•{c}^{2}({H}_{2})}$
(2)下列各项中,不能够说明该反应已达到平衡的是bd
a.恒温、恒容条件下,容器内的压强不发生变化
b.恒温、恒容条件下,容器内的气体密度不发生变化
c.一定条件下,CO、H2和CH3CH的浓度保持不变
d.一定条件下,单位时间内生成1mol H2,同时生成1mol CH3OH
e.混合气体的平均相对分子质量不再变化
(3)下表所列数据是该反应在不同温度下的化学平衡常数(K)
①若容器容积不变,可增加甲醇产率的措施是降低温度或及时分离甲醇.
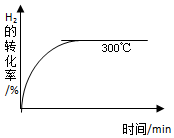
②其他条件相同时,在上述三个温度下分别发生该反应.300℃时,H2的转化率随时间的变化如图所示,请补充完成250℃时H2的转化率随时间的变化示意图.
(4)已知在常温常压下:
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=-a kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H=-b kJ•mol-1
③H2O(g)=H2O(l)△H=-c kJ•mol-1
则 CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=$\frac{b-a-4c}{2}$ kJ•mol-1.
 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)?CH3OH(g)(1)该反应的平衡常数表达式K=$\frac{c(C{H}_{3}OH)}{c(CO)•{c}^{2}({H}_{2})}$
(2)下列各项中,不能够说明该反应已达到平衡的是bd
a.恒温、恒容条件下,容器内的压强不发生变化
b.恒温、恒容条件下,容器内的气体密度不发生变化
c.一定条件下,CO、H2和CH3CH的浓度保持不变
d.一定条件下,单位时间内生成1mol H2,同时生成1mol CH3OH
e.混合气体的平均相对分子质量不再变化
(3)下表所列数据是该反应在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②其他条件相同时,在上述三个温度下分别发生该反应.300℃时,H2的转化率随时间的变化如图所示,请补充完成250℃时H2的转化率随时间的变化示意图.
(4)已知在常温常压下:
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=-a kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H=-b kJ•mol-1
③H2O(g)=H2O(l)△H=-c kJ•mol-1
则 CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=$\frac{b-a-4c}{2}$ kJ•mol-1.
10.25℃时,某一元酸(HB)对应的盐NaB的水溶液呈碱性,下列叙述正确的是( )
| A. | 0.1 mol/L NaB溶液中水电离的OH-浓度大于10-7 mol/L | |
| B. | NaB溶液中:c(Na+)>c(B-)>c(H+)>c(OH-) | |
| C. | NaB溶液中:c(Na+)+c(H+)=c(HB)+c(B-) | |
| D. | HB的电离方程式为:HB═H++B- |