题目内容
合成氨所需的氢气可用煤和水作原料经多步反应制得,其中的一步反应为:CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,反应达到平衡后,为提高CO的转化率,下列措施中正确的是( )
| A、增大CO的浓度 | B、降低温度 |
| C、升高温度 | D、增大压强 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:提高CO的转化率可以使平衡正向进行,根据化学平衡移动原理来回答判断,注意只增大CO的浓度,平衡向正反应方向移动,但CO的转化率会降低.
解答:
解:A、增大CO的浓度,化学平衡向着正方向进行,但是一氧化碳的转化率降低,故A错误;
B、正反应为放热反应,降低温度,化学平衡向正反应方向移动,CO的转化率提高,故B正确;
C、正反应为放热反应,升高温度,化学平衡向逆反应方向移动,CO的转化率降低,故C错误;
D、该反应前后气体的体积不变,增加压强,该平衡会不会发生移动,CO的转化率不变,故D错误;
故选B.
B、正反应为放热反应,降低温度,化学平衡向正反应方向移动,CO的转化率提高,故B正确;
C、正反应为放热反应,升高温度,化学平衡向逆反应方向移动,CO的转化率降低,故C错误;
D、该反应前后气体的体积不变,增加压强,该平衡会不会发生移动,CO的转化率不变,故D错误;
故选B.
点评:本题考查学生化学平衡移动原理的应用方面的知识,属于基本知识的考查,注意知识的积累是解题的关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
欲配制100mL 1.0mol?L-1 Na2SO4溶液,正确的方法是( )
| A、将14.2 g Na2SO4溶于100 mL水中 |
| B、将14.2 g Na2SO4?10H2O溶于少量水中,再用水稀释至100 mL |
| C、将20 mL 5.0 mol?L-1 Na2SO4溶液用水稀释至100 mL |
| D、将50 mL 2.0 mol?L-1 Na2SO4溶液注入100 mL容量瓶中再加水至100 mL |
下列说法错误的是( )
| A、常温下氨基酸都晶体 |
| B、石油和煤都是烃类物质 |
| C、油酸是单不饱和高级脂肪酸 |
| D、HNO3能与甘油、纤维素等在一定条件下发生反应 |
下列各反应达到化学平衡后,加压或降温都能使化学平衡向逆反应方向移动的是( )
| A、2NO2?N2O4 (正反应为放热反应) |
| B、C(s)+CO2?2CO (正反应为吸热反应) |
| C、N2+3H2?2NH3 (正反应为放热反应) |
| D、H2S?H2+S(S) (正反应为吸热反应) |
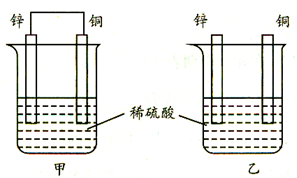 将纯铜片和纯锌片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
将纯铜片和纯锌片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )| A、两烧杯中铜片表面均无气泡产生 |
| B、甲中铜片是正极,电极反应:2H++2e→H2↑;乙中锌片是负极,电极反应:Zn-2e→Zn2+ |
| C、两烧杯中的pH值均增大 |
| D、产生的气泡速率甲比乙慢 |
下列说法中,不正确的是( )
| A、金属的冶炼,就是利用氧化还原反应原理,在一定条件下将金属从其化合物中还原出来 |
| B、冶炼金属时,必须加入一种物质作为还原剂 |
| C、金属由化合态变为游离态,都是被还原 |
| D、金属单质被发现和应用得越早,其活动性一般越弱 |
下列说法中错误的是( )
| A、金属晶体的四种堆积模型中,六方最密堆积和面心立方最密堆积的空间利用率最高 |
| B、通过手性合成的方法,可以只得到一种或者主要只得到一种手性分子 |
| C、金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 |
| D、分子形成氢键一定使物质的熔沸点升高 |
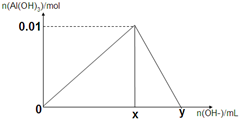 将3mol/L NaOH溶液滴入到25mL一定浓度的AlCl3溶液中.如图是整个过程的数学分析曲线.其中横轴表示加入OH-的体积,纵轴表示产生的Al(OH)3沉淀物质的量.据图示回答下列问题:
将3mol/L NaOH溶液滴入到25mL一定浓度的AlCl3溶液中.如图是整个过程的数学分析曲线.其中横轴表示加入OH-的体积,纵轴表示产生的Al(OH)3沉淀物质的量.据图示回答下列问题: