题目内容
19.对于放热反应Zn+H2SO4═ZnSO4+H2↑,下列叙述正确的是( )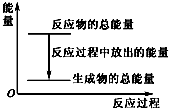
| A. | 反应过程中的能量关系可用如图表示 | |
| B. | 1 mol Zn的能量大于1 mol H2的能量 | |
| C. | 若将其设计为原电池,则锌作正极 | |
| D. | 若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L |
分析 A、根据放热反应中反应物的总能量大于生成物的总能量;
B、放热反应中反应物的总能量大于生成物的总能量;
C、原电池的负极失去电子;
D、根据总反应方程式以及气体的体积与状态有关来计算;.
解答 解:A、放热反应Zn+H2SO4═ZnSO4+H2↑,则反应物的总能量大于生成物的总能量,故A正确;
B、放热反应中反应物的总能量大于生成物的总能量,则无法比较1molZn与1 molH2的能量,故B错误;
C、Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g)的反应中锌失去电子,化合价升高,作原电池的负极,故C错误;
D、Zn+H2SO4 =ZnSO4 +H2↑
65g 22.4L
65g 11.2L
所以32.5g锌溶解时,正极放出气体在标况下11.2L,不一定为11.2L,故D错误;
故选:A.
点评 本题主要考查原电池原理、化学反应中的能量以及化学计算等,难度不大,根据课本知识即可完成.

练习册系列答案
相关题目
9.对于某些离子的检验及结论一定正确的是( )
| A. | 通入Cl2后,溶液变为黄色,加淀粉液后溶液变蓝,则原溶液中一定有I- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液中一定有SO42- | |
| C. | 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32- | |
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
7.下列有关能源和能量转换的叙述正确的是( )
| A. | 推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应 | |
| B. | 乙醇和汽油都是可再生能源,应大力推广“乙醇汽油” | |
| C. | 普通锌锰干电池不含环境污染物,用完后可以随意扔掉,使用方便 | |
| D. | 燃料电池是利用燃料燃烧,将化学能转化为热能,然后再转化为电能的化学电源 |
4.某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1:2,下列说法正确的是( )
| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:4 | ||
| C. | 分子中可能含有氧原子 | D. | 此有机物的最简式为CH4 |
11.下列化学式表示的物质一定为纯净物的是( )
| A. | C3H8 | B. | C4H10 | C. | C12H22O11 | D. | C |
16.下列离子方程式中,正确的是( )
| A. | 水玻璃中通入足量的CO2:SiO32-+2CO2+2H2O═H2SiO3 (胶体)+2CO32- | |
| B. | 氯化亚铁溶液中通入足量的Cl2:2Fe2++Cl2═2Fe3++2Cl- | |
| C. | NaHCO3溶液中加入足量NaHSO4溶液:2H++CO32-═CO2↑+H2O | |
| D. | 碳酸氢钠溶液与少量石灰水反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
 .用系统法命名为:2-甲基丁烷.
.用系统法命名为:2-甲基丁烷.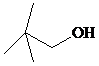 ,其名称(系统法命名)为2,2-二甲基-1-丙醇,1mol醇A与足量钠反应,可生成H2的体积为11.2L(标况)
,其名称(系统法命名)为2,2-二甲基-1-丙醇,1mol醇A与足量钠反应,可生成H2的体积为11.2L(标况)
 .
.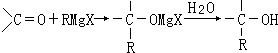

 ,
,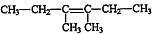 ;
;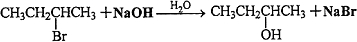 ,I→J
,I→J .
.