题目内容
1.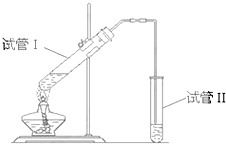 如图所示装置,该装置用于制备少量乙酸乙酯,请回答:
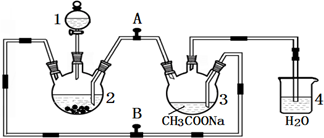
如图所示装置,该装置用于制备少量乙酸乙酯,请回答:①试管Ⅰ中盛有的试剂是浓硫酸、乙酸和乙醇;
②试管Ⅱ中的试剂是饱和Na2CO3溶液;它的作用是溶解乙醇、中和乙酸,降低乙酸乙酯的溶解度,便于分层;
③浓硫酸的作用是催化剂、吸水剂;
④化学方程式为CH3CH2OH+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O.
分析 实验室用乙醇、乙酸在浓硫酸作用下,加热发生酯化反应生成乙酸乙酯,乙酸乙酯不溶于饱和碳酸钠溶液,乙酸可与碳酸钠溶液反应,试管Ⅱ中盛有饱和碳酸钠溶液,注意防止倒吸,以此解答该题.
解答 解:①制备乙酸乙酯,需要浓硫酸、乙酸和乙醇,故答案为:乙醇;
②实验室用饱和碳酸钠溶液吸收,因乙酸乙酯不溶于饱和碳酸钠溶液,且饱和碳酸钠溶液可起到除去乙酸和乙醇的作用,饱和碳酸钠溶液可溶解乙醇,中和乙酸,降低乙酸乙酯的溶解度,
故答案为:饱和Na2CO3溶液;乙酸;乙酸乙酯;
③反应中浓硫酸起到催化剂的作用,因反应为可逆反应,且生成水,浓硫酸还起到吸收水的作用,有利于平衡正向移动,
故答案为:催化剂、吸水剂;
④发生反应的化学方程式为CH3CH2OH+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O,
故答案为:CH3CH2OH+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O.
点评 本题考查有机物的制备实验,为高频考点,侧重分析与实验能力的考查,把握制备实验操作、混合物分离提纯、有机物的性质为解答的关键,注意混合物的加入顺序,题目难度不大.

练习册系列答案
相关题目
5.氢氧化钠固体配制480mL0.1mol/LNaOH溶液时,下列有关说法错误的是( )
| A. | 用到的玻璃仪器有:玻璃棒、胶头滴管、500mL容量瓶、烧杯 | |
| B. | 需要称量氢氧化钠固体1.92g | |
| C. | 没有等溶液冷却就转移将导致所配溶液浓度偏高 | |
| D. | 洗净的容量瓶不需要干燥就能使用,但使用前需检漏 |
6.系列物质在水溶液中的电离方程式书写错误的是( )
①NaHSO3=Na++H++SO32-
②NaHSO4=Na++H++SO42-
③H2SO4=2H++SO42-
④Ca(OH)2=Ca2++(OH-)2.
①NaHSO3=Na++H++SO32-
②NaHSO4=Na++H++SO42-
③H2SO4=2H++SO42-
④Ca(OH)2=Ca2++(OH-)2.
| A. | ①② | B. | ① | C. | ③④ | D. | ①④ |
3.阿伏加德罗常数约为6.02×1023 mol-1,下列说法正确的是( )
| A. | 2.3 g钠与足量丙三醇反应,转移电子数为0.3×6.02×1023 | |
| B. | 标准状况下,22.4 L乙醇的共价键数为8×6.02×1023 | |
| C. | 标准状况下,5.6 L甲醛所含的电子数为4×6.02×1023 | |
| D. | 100 mL 1 mol•L-1醋酸溶液中,H+的个数为0.1×6.02×1023 |
10.有关Al与NaOH溶液反应的说法中正确的是( )
| A. | 铝是还原剂,其氧化产物是H2 | B. | NaOH是氧化剂,其还原产物是H2 | ||
| C. | 铝是还原剂,H2O和NaOH都是氧化剂 | D. | H2O是氧化剂,Al被氧化 |
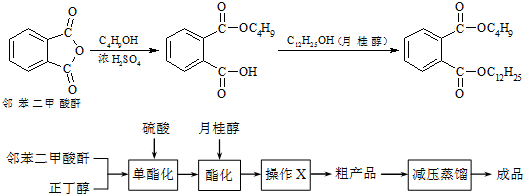
10.邻苯二甲酸丁基月桂酯是一种淡黄色透明油状液体,密度约0.97g/cm3,常用作聚氯乙烯等树脂的增塑剂.工业上生产原理和工艺流程如下:
有关物质的物理性质见下表:
某实验小组的同学模拟工业生产的工艺流程,用如图所示装置制取少量邻苯二甲酸丁基月桂酯,图中夹持和加热装置已略去.主要操作步骤如下: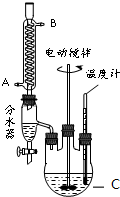
②向三颈烧瓶内加入30g 邻苯二甲酸酐、16g 正丁醇以及少量浓硫酸.
②搅拌,升温至105℃,持续搅拌反应1小时.
③冷却至室温,加入40g 月桂醇,升温至160℃,搅拌、保温至反应结束.
④冷却至室温,将反应混合物倒出.
⑤通过工艺流程中的操作X,得到粗产品.
请回答下列问题:
(1)仪器C的名称三颈烧瓶.冷凝管中冷水应从A进.
(2)步骤③中判断反应已结束的方法是分水器中的水不再增加.
(3)步骤⑤中操作X可除去少量未反应的邻苯二甲酸酐及正丁醇,操作X包括先用饱和碳酸钠洗涤、分液,再用蒸馏水洗涤、分液(洗涤、分液).
(4)工艺流程中减压蒸馏的目的是降低沸点,防止高温下发生副反应,致使产品不纯.
(5)实验结果表明步骤②、③产率都比较高,原因是生成的水蒸出冷凝成液态后通过分水器从体系中分离出去,促进反应.

有关物质的物理性质见下表:
| 化合物 | 溶解性 | 熔点 | 沸点 |
| 邻苯二甲酸酐 | 微溶于冷水、乙醚,易溶于热苯、乙醇、乙酸 | 131.6℃ | 295℃ |
| 正丁醇 | 微溶于水,溶于乙醇、醚、多数有机溶剂 | -88.9℃ | 117.5℃ |
| 月桂醇 | 不溶于水,溶于醇、醚 | 24 | 259℃ |
| 邻苯二甲酸丁基月桂酯 | 不溶于水,溶于多数有机溶剂 | 不祥 | 202~210℃ |

②向三颈烧瓶内加入30g 邻苯二甲酸酐、16g 正丁醇以及少量浓硫酸.
②搅拌,升温至105℃,持续搅拌反应1小时.
③冷却至室温,加入40g 月桂醇,升温至160℃,搅拌、保温至反应结束.
④冷却至室温,将反应混合物倒出.
⑤通过工艺流程中的操作X,得到粗产品.
请回答下列问题:
(1)仪器C的名称三颈烧瓶.冷凝管中冷水应从A进.
(2)步骤③中判断反应已结束的方法是分水器中的水不再增加.
(3)步骤⑤中操作X可除去少量未反应的邻苯二甲酸酐及正丁醇,操作X包括先用饱和碳酸钠洗涤、分液,再用蒸馏水洗涤、分液(洗涤、分液).
(4)工艺流程中减压蒸馏的目的是降低沸点,防止高温下发生副反应,致使产品不纯.
(5)实验结果表明步骤②、③产率都比较高,原因是生成的水蒸出冷凝成液态后通过分水器从体系中分离出去,促进反应.
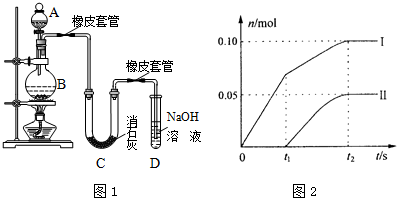
 醋酸亚铬水合物
醋酸亚铬水合物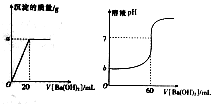 室温下,某同学为测量硫酸和盐酸混合溶液中溶质的浓度进行如下实验:取混合酸20mL放入锥形瓶中,逐滴滴人0.05mol•L-1的Ba(OH)2溶液,实验记录如下:(1g3=0.5)
室温下,某同学为测量硫酸和盐酸混合溶液中溶质的浓度进行如下实验:取混合酸20mL放入锥形瓶中,逐滴滴人0.05mol•L-1的Ba(OH)2溶液,实验记录如下:(1g3=0.5)