题目内容
下列离子方程式书写正确的是( )
| A、硫酸镁与氢氧化钾反应:MgSO4+2OH-=Mg(OH)2↓+SO42- |
| B、氧化铜与稀硫酸反应:O2-+2H+=H2O |
| C、碳酸钙与醋酸反应:CO32-+2H+=CO2↑+H2O |
| D、氧化亚铁溶于稀盐酸:FeO+2H+=Fe2++H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.硫酸镁为可溶性盐应拆成离子形式;
B.氧化铜不能拆;
C.碳酸钙难溶性盐,醋酸是弱电解质,都应保留化学式;
D.氧化亚铁溶于稀盐酸反应生成氯化亚铁和水.
B.氧化铜不能拆;
C.碳酸钙难溶性盐,醋酸是弱电解质,都应保留化学式;
D.氧化亚铁溶于稀盐酸反应生成氯化亚铁和水.
解答:
解:A.硫酸镁与氢氧化钾反应的离子方程式:Mg2++2OH-=Mg(OH)2↓,故A错误;
B.氧化铜与稀硫酸反应的离子方程式:CuO+2H+=H2O+Cu2+,故B错误;
C.碳酸钙与醋酸反应离子方程式:CaCO3+2CH3COOH=CO2↑+Ca2++2CH3COO-+H2O,故C错误;
D.氧化亚铁溶于稀盐酸反应的离子方程式:FeO+2H+=Fe2++H2O,故D正确;
故选:D.
B.氧化铜与稀硫酸反应的离子方程式:CuO+2H+=H2O+Cu2+,故B错误;
C.碳酸钙与醋酸反应离子方程式:CaCO3+2CH3COOH=CO2↑+Ca2++2CH3COO-+H2O,故C错误;
D.氧化亚铁溶于稀盐酸反应的离子方程式:FeO+2H+=Fe2++H2O,故D正确;
故选:D.
点评:本题考查了离子方程式书写及正误判断,侧重离子方程式书写时化学式的拆分的考查,熟记:气体、水、不溶于水的化合物、氧化物、单质、弱电解质(弱酸,弱碱)都不拆,可溶性盐、强酸、强碱必须拆是解题的关键.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、氯化钠在电流作用下电离成钠离子和氯离子 |
| B、硫酸钡难溶于水,但硫酸钡属于电解质 |
| C、溶于水后能电离出氢离子的化合物都是酸 |
| D、1mol HCl气体中的粒子数与0.5mol/L盐酸中溶质粒子数相等 |
 如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )| A、原子半径:R>Y>X |
| B、气态氢化物的稳定性:R<W |
| C、WX3和水反应形成的化合物具有挥发性 |
| D、Z的单质能和Y的最高价氧化物的水化物反应 |
 某化学反应2A(g)?B(g),反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )
某化学反应2A(g)?B(g),反应过程中能量变化如图所示(图中E1 表示正反应的活化能,E2 表示逆反应的活化能).下列有关叙述正确的是( )| A、该反应为放热反应 |
| B、催化剂无法改变该反应的焓变 |
| C、催化剂不能改变反应路径,但能降低该反应的活化能 |
| D、生成物B比反应反应物A更稳定 |
已知4NH3(g)+5O2(g)?4NO(g)+6H2O(g).若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)来表示,则下列关系正确的是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
在下列反应中,HCl 既体现酸性又体现还原性的是( )
| A、NaOH+HCl=NaCl+H2O | ||||
| B、Zn+2HCl=ZnCl2+H2↑ | ||||
C、MnO2+4HCl(浓)
| ||||
| D、CuO+2HCl=CuCl2+H2O |
下列物质中由于水解使溶液的pH小于7的是( )
| A、NaHCO3 |
| B、NH4Cl |
| C、Na2SO4 |
| D、NaHSO4 |
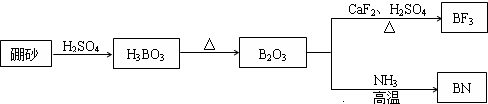
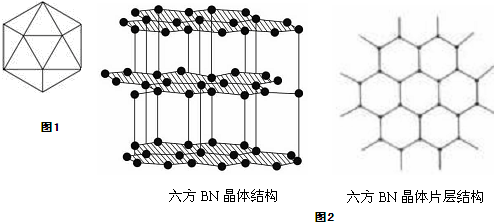
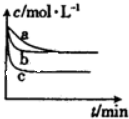 1000℃时,硫酸钠可与氢气发生反应:Na2SO4(s)+4H2(g)?Na2S(s)+4H2O(g).请回答下列问题:
1000℃时,硫酸钠可与氢气发生反应:Na2SO4(s)+4H2(g)?Na2S(s)+4H2O(g).请回答下列问题: