题目内容
某溶液中含有大量Fe3+、Fe3+、Mg2+和NH4+,其c(H+)=10-2mol?L-1,在该溶液中可以大量存在的阴离子是( )
| A、SO42- |
| B、NO3- |
| C、SCN- |
| D、CO32- |
考点:离子共存问题
专题:
分析:溶液中c(H+)=10-2mol?L-1,则溶液呈酸性,则溶液中不能存在和这几种离子反应的离子,据此分析解答.
解答:
解:A.硫酸根离子和这几种离子都不反应,所以能共存,故A正确;
B.酸性条件下,硝酸根离子和亚铁离子发生氧化还原反应而不能共存,故B错误;
C.铁离子和硫氰根离子反应生成络合物而不能共存,故C错误;
D.镁离子、铁离子和亚铁离子都与碳酸根离子发生反应,所以不能共存,故D错误;
故选A.
B.酸性条件下,硝酸根离子和亚铁离子发生氧化还原反应而不能共存,故B错误;
C.铁离子和硫氰根离子反应生成络合物而不能共存,故C错误;
D.镁离子、铁离子和亚铁离子都与碳酸根离子发生反应,所以不能共存,故D错误;
故选A.
点评:本题考查离子共存,为高考高频点,明确离子性质及离子共存条件即可解答,侧重考查复分解反应和络合反应,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知,有机化合物A只由碳、氢两种元素组成且能使溴水褪色,其产量可以用来衡量一个国家石油化工发展水平.A、B、C、D、E有如下关系:则下列推断不正确的是( )


| A、B+D→E的化学方程式为:CH3CH2OH+CH3COOH→CH3COOC2H5 |
| B、D中含有的官能团为羧基,利用D物质可以清除水壶中的水垢 |
| C、物质C的结构简式为CH3CHO,E的名称为乙酸乙酯 |
| D、鉴别A和甲烷可选择使用酸性高锰酸钾溶液 |
PM2.5是指大气中直径接近于2.5×10-6 m的颗粒物,下列有关PM2.5说法不正确的是( )
| A、PM2.5表面积大能吸附大量的有毒、有害物质 |
| B、PM2.5在空气中形成气溶胶 |
| C、实施绿化工程,可以有效地防治PM2.5污染 |
| D、研制开发燃料电池汽车,降低机动车尾气污染,某种程度上可以减少PM2.5污染 |
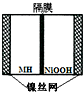 如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池 (MH-Ni碱性电池).下列有关说法不正确的是( )
如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池 (MH-Ni碱性电池).下列有关说法不正确的是( )| A、放电时正极反应为:NiOOH+H2O+e-=Ni(OH)2+OH- |
| B、放电时负极反应为:MH+OH--2e-=H2O+M+ |
| C、充电时氢氧根离子移向阳极,要参与电极反应 |
| D、充电时电池的正极连接直流电源的正极,得到电子发生还原反应 |
下列变化需要加入还原剂才能实现的转化是( )
| A、Fe2+→Fe3+ |
| B、H2SO4→SO2 |
| C、H2S→SO2 |
| D、HCO3-→CO2 |
 实验室要测定某氯化铜溶液中溶质的质量分数,取该溶液100g,逐滴滴加一定溶质质量分数的氢氧化钠溶液,反应过程中生成沉淀的质量与加入氢氧化钠溶液质量的关系如图所示.(反应的化学方程式:2NaOH+CuCl2=Cu(OH)2↓+2NaCl)求:
实验室要测定某氯化铜溶液中溶质的质量分数,取该溶液100g,逐滴滴加一定溶质质量分数的氢氧化钠溶液,反应过程中生成沉淀的质量与加入氢氧化钠溶液质量的关系如图所示.(反应的化学方程式:2NaOH+CuCl2=Cu(OH)2↓+2NaCl)求: 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: