题目内容
标准状况下,将3.36升CO2 气体通入200mL 1.00mol/L NaOH溶液中,充分反应后溶液中Na2CO3 和NaHCO3 的浓度比为多少?
考点:化学方程式的有关计算
专题:
分析:设反应后溶液中Na2CO3 和NaHCO3 的物质的量分别为xmol、ymol,根据钠离子、碳原子守恒列方程计算反应应后溶液中Na2CO3 和NaHCO3 的物质的量,再根据c=
可知,浓度之比等于其物质的量之比.
| n |
| V |
解答:
解:3.36L二氧化碳物质的量为
=0.15mol,NaOH的物质的量为0.2L×1mol/L=0.2mol,
设反应后溶液中Na2CO3 和NaHCO3 的物质的量分别为xmol、ymol,根据钠离子、碳原子守恒,则:
解得x=0.05,y=0.1
故反应后溶液中Na2CO3 和NaHCO3 的浓度比为0.05mol:0.1mol=1:2,
答:反应后溶液中Na2CO3 和NaHCO3 的浓度比为1:2.
| 3.36L |
| 22.4L/mol |
设反应后溶液中Na2CO3 和NaHCO3 的物质的量分别为xmol、ymol,根据钠离子、碳原子守恒,则:
|
解得x=0.05,y=0.1
故反应后溶液中Na2CO3 和NaHCO3 的浓度比为0.05mol:0.1mol=1:2,
答:反应后溶液中Na2CO3 和NaHCO3 的浓度比为1:2.
点评:本题考查化学方程式有关计算,难度不大,注意利用守恒法解答,侧重考查学生分析计算能力.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
某溶液中含有大量Fe3+、Fe3+、Mg2+和NH4+,其c(H+)=10-2mol?L-1,在该溶液中可以大量存在的阴离子是( )
| A、SO42- |
| B、NO3- |
| C、SCN- |
| D、CO32- |
下列叙述错误的是( )
| A、H2SO4的摩尔质量是98 |
| B、H2SO4的摩尔质量与NA个H2SO4分子的质量相等 |
| C、等质量的O2和O3中所含氧原子数相同 |
| D、等物质的量的CO和CO2中所含碳原子数相同 |
某溶液由NaCl、MgCl2、Al2(SO4)3、Na2SO4组成,已知c(Na+)=0.4mol/L,c(Al3+)=0.2mol/L,c(Mg2+)=0.1mol/L,c(Cl-)=0.3mol/L,则SO42-物质的量浓度为( )
| A、0.3mol/L |
| B、0.4mol/L |
| C、0.45mol/L |
| D、0.55mol/L |
甲烷在足量氧气中燃烧生成二氧化碳和水,由该实验事实可以得出的结论是( )
| A、甲烷的分子式为CH4 |
| B、甲烷中含有碳元素和氢元素 |
| C、甲烷中只含碳元素和氢元素 |
| D、甲烷的化学性质比较稳定 |
下列物质的性质属于化学性质的是( )
| A、颜色、状态 | B、溶解性 |
| C、密度、硬度 | D、可燃性 |
下列叙述中,能证明某物质是弱电解质的是( )
| A、熔化时不导电 |
| B、易溶于水 |
| C、水溶液的导电能力很差 |
| D、溶液中已电离的离子和未电离的分子共存 |
阿魏酸在食品、医药等方面有广泛用途.一种合成阿魏酸的反应可表示为下列说法正确的是( )
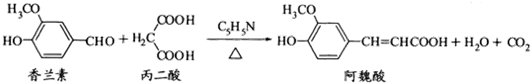

| A、香兰素、阿魏酸均可与溴水反应,且反应类型完全相同 |
| B、香兰素、阿魏酸均可与NaHCO3、NaOH溶液反应 |
| C、与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有2种 |
| D、通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应 |