��Ŀ����
18�� ��������Ԫ�أ�����B��C��D��EΪ����������Ԫ�أ�F��GΪ��������Ԫ�أ����ǵ�ԭ����������������������������Ϣ���ش�����
��������Ԫ�أ�����B��C��D��EΪ����������Ԫ�أ�F��GΪ��������Ԫ�أ����ǵ�ԭ����������������������������Ϣ���ش�����| BԪ��ԭ�ӵĺ���p��������s��������1 |
| Cԭ�ӵĵ�һ�����ĵ����ֱܷ��ǣ� I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| Dԭ�Ӻ�������p���ȫ������� |
| EԪ�ص������������������IJ�Ϊ4 |
| F ��ǰ������ԭ�ӵ��ӹ����ʾʽ�е�����������Ԫ�� |
| G�����ڱ��ĵ�ʮһ�� |
��2��C��������������Ԫ��ԭ�ӵĵ�һ�������ɴ�С��˳����Mg��Al��Na��
��3����DE3����ԭ�ӵ��ӻ���ʽΪsp3�ӻ����÷����еļ��DZ�����DE4+�еļ���С��ԭ���ǹµ��Ӷ���ɼ����ӶԵ��ų����������ڳɼ����Ӷ�֮����ų�������
�ڽ�E�ĵ���ͨ�뵽��Ѫ��{K4[Fe��CN��6]}��Һ�У��ɵõ���Ѫ��{K3[Fe��CN��6]}���÷�Ӧ�����ӷ���ʽΪ[Fe��CN��6]4-+Cl2=2[Fe��CN��6]3-+2Cl-
����֪��E��һ�ֻ�������������ⷢ�����·�Ӧ������ƽ����H2O2+
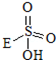 ��
��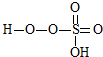 +HE ����д�����������ʵĽṹʽ��
+HE ����д�����������ʵĽṹʽ����4��Fλ��d�����۵����Ų�ʽΪ3d54s1��
��5��G���ʾ�����ԭ�ӵĶѻ���ʽΪ�����������ܶѻ�����ͼ��������ÿ��ԭ�ӵ���λ��Ϊ12�����辧���߳�Ϊa��ԭ�Ӱ뾶Ϊr����ʽ��ʾ�þ����Ŀռ�������Ϊ$\frac{\sqrt{2}��}{6}$��
���� B��C��D��EΪ����������Ԫ�أ�F��GΪ��������Ԫ�أ����ǵ�ԭ��������������
BԪ��ԭ�ӵĺ���p��������s��������1��B��2�����Ӳ㣬Ϊ1s22s22p3����BΪNԪ�أ�
��Cԭ�ӵĵ�һ�����ĵ��������ݿ�֪�����������ܾ�������C����+2�ۣ����ڢ�A�壬ԭ����������NԪ�أ���CΪMgԪ�أ�
D���ڵ������ڣ�Dԭ�Ӻ�������p���ȫ���������������Ų�Ϊ3s23p3����DΪPԪ�أ�
E���ڵ������ڣ�EԪ�ص������������������IJ�Ϊ4��E���ڵڢ�A�壬��EΪClԪ�أ�
F ��ǰ������ԭ�ӵ��ӹ����ʾʽ�е�����������Ԫ�أ������е�δ�ɶԵ�������࣬����Χ�����Ų�Ϊ3d54s1��ΪCrԪ�أ�
G�����ڱ��ĵ�11�У���Eλ�ڵ������ڵ�IB�壬ΪCuԪ�أ��ݴ˴��⣮
��� �⣺B��C��D��EΪ����������Ԫ�أ�F��GΪ��������Ԫ�أ����ǵ�ԭ��������������
BԪ��ԭ�ӵĺ���p��������s��������1��B��2�����Ӳ㣬Ϊ1s22s22p3����BΪNԪ�أ�
��Cԭ�ӵĵ�һ�����ĵ��������ݿ�֪�����������ܾ�������C����+2�ۣ����ڢ�A�壬ԭ����������NԪ�أ���CΪMgԪ�أ�
D���ڵ������ڣ�Dԭ�Ӻ�������p���ȫ���������������Ų�Ϊ3s23p3����DΪPԪ�أ�
E���ڵ������ڣ�EԪ�ص������������������IJ�Ϊ4��E���ڵڢ�A�壬��EΪClԪ�أ�
F ��ǰ������ԭ�ӵ��ӹ����ʾʽ�е�����������Ԫ�أ������е�δ�ɶԵ�������࣬����Χ�����Ų�Ϊ3d54s1��ΪCrԪ�أ�
G�����ڱ��ĵ�11�У���Eλ�ڵ������ڵ�IB�壬ΪCuԪ�أ�
��1��BΪNԪ�أ�B��̬ԭ����������ߵĵ���Ϊ2p����ϵ��������ӣ���������ڿռ���3������ԭ�ӹ���������Σ�
�ʴ�Ϊ��3�����壻
��2��Ԫ�طǽ�����Խǿ����һ������Խ��CΪMgԪ�أ������s��������������ӣ������ȶ��ṹ���������ĵ�һ�����ܸ���������������Ԫ��ԭ�ӵĵ�һ�����ܣ����Ե�һ�������ɴ�С��˳����Mg��Al��Na��
�ʴ�Ϊ��Mg��Al��Na��
��3����DE3ΪPCl3��PCl3��Pԭ�ӹµ��Ӷ���Ϊ1����3���Ҽ�����Ϊsp3�ӻ���DE4+ΪNH4+�����������д���һ�Թµ��Ӷԣ��µ��Ӷ���ɼ����ӶԵ��ų����������ڳɼ����Ӷ�֮����ų����������ʰ����м��Ǵ���笠��м��ǣ�
�ʴ�Ϊ��sp3���µ��Ӷ���ɼ����ӶԵ��ų����������ڳɼ����Ӷ�֮����ų���������
��E�ĵ���Ϊ��������ӦΪΪ�����ͻ�Ѫ�Σ�������Ϊ��Ѫ�Σ��ʴ˷�Ӧ�����ӷ�Ӧ����ʽΪ��[Fe��CN��6]4-+Cl2=2[Fe��CN��6]3-+2Cl-��
�ʴ�Ϊ��[Fe��CN��6]4-+Cl2=2[Fe��CN��6]3-+2Cl-��
���������ķ���ʽ��֪���˷�ӦΪ˫��ˮ�е�H��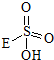 ��ȥ��E�IJ���ȡ�����ɵģ������ɵ���һ�ֲ���Ľṹ��ʽΪ��
��ȥ��E�IJ���ȡ�����ɵģ������ɵ���һ�ֲ���Ľṹ��ʽΪ��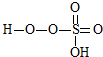 ��
��
�ʴ�Ϊ��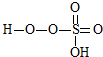 ��
��
��4��FΪCrԪ�أ���25��Ԫ�أ�λ�ڵ������ڵ�VB�壬�������Ϊd���ӣ�Ϊd��Ԫ�أ��۵����Ų�ʽΪ3d54s1��
�ʴ�Ϊ��d��3d54s1��
��5����ͼ��֪������Ϊ���������ѻ����Զ����ԭ�ӷ�����λ�����ĵ�ԭ����֮���������1������ԭ��Ϊ12���湲�ã�����λ��Ϊ12��Cuԭ�Ӱ뾶Ϊr����Խ���������Cuԭ�����ڣ���Խ��߳���=4r�����ⳤ=$2\sqrt{2}$r���������=��$2\sqrt{2}$r��3���þ�����Cuԭ�Ӹ���=8��$\frac{1}{8}$+6��$\frac{1}{2}$=4��ÿ����ԭ�����=$\frac{4}{3}$��r3���þ����к���4��Alԭ�ӣ����Ծ�����������ԭ�����=4��$\frac{4}{3}$��r3���ռ�������=$\frac{����ͭԭ�����}{�������}$=$\frac{4��\frac{4��r3}{3}}{��{2\sqrt{2}r��}^{3}}$=$\frac{\sqrt{2}��}{6}$��
�ʴ�Ϊ��12�� $\frac{\sqrt{2}��}{6}$��
���� ���⿼�����ʽṹ�����ʣ��漰Ԫ�������ɡ��ӻ��������������Ų��������ṹ�����ȣ�ע��Ե�����ͻ������⣬����������Ҫѧ������һ������ѧ����������ռ����������Ѷ��еȣ�

 ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д�
ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д�| A�� | ��Ԫ�ص����ǵ��� | |
| B�� | ��Ԫ�ص�����һ���������������ᷴӦ | |
| C�� | ��Ԫ�ص��������ˮ�����Լ��� | |
| D�� | ��Ԫ�ص�����������Ӧ��ˮ����Ϊ���� |
| A�� | 0.1 mol•L-1 CH3COONa��Һ��0.1 mol•L-1HCl��Һ�������ϣ�c��Na+��=c��Cl-����c��CH3COO-����c��OH-�� | |
| B�� | 0.1 mol•L-1 NH4Cl��Һ��0.1 mol•L-1��ˮ�������ϣ�pH��7����c��NH3•H2O����c��NH4+����c��Cl-����c��OH-�� | |
| C�� | 0.1 mol•L-1Na2CO3��Һ��0.1 mol•L-1NaHCO3��Һ�������ϣ�$\frac{3}{2}$c��Na+��=c��CO32-��+c��HCO3-��+c��H2CO3�� | |
| D�� | 0.1 mol•L-1Na2C2O4��Һ��0.1 mol•L-1HCl��Һ�������ϣ�H2C2O4Ϊ��Ԫ���ᣩ��2c��C2O42-��+c��HC2O42-��+c��OH-��=c��Na+��+c��H+�� |
| A�� | ����SO2ͨ��Ca��ClO��2��Һ�У�SO2+H2O+Ca2++2ClO-�TCaSO3��+2HClO | |
| B�� | ��ϡ��ˮ��ͨ������CO2��2NH3•H2O+CO2�T2NH4++CO32-+H2O | |
| C�� | ��ϡHCl��Һ�ܽ�FeS���壺FeS+2H+�TFe2++H2S�� | |
| D�� | Cl2��ˮ��Ӧ��Cl2+H2O�THCl+HClO |
| A�� | �����оƬ�����Ԫ��λ�ڵ�14���� | |
| B�� | ��10����Ԫ��ȫ���ǽ���Ԫ�� | |
| C�� | ��3����Ԫ�ص�������� | |
| D�� | ֻ�е�2����Ԫ�ص�ԭ���������2������ |
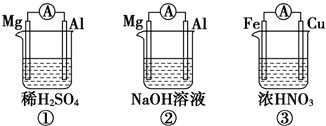
| A�� | �٢���Mg������������Fe������ | |
| B�� | ����Al����������缫��ӦʽΪAl-3e-=Al3+ | |
| C�� | ����Fe���������缫��ӦʽΪFe-2e-=Fe2+ | |
| D�� | ���٢���ת�Ƶĵ�������ͬ����٢��в�����H2����Ҳһ����ͬ |
| A�� | ʳ����Ҫ�ɷ��Ǵ��ᣬ����һ������ | |
| B�� | �����ж�����������ɱ������ | |
| C�� | ����ϩ������Ʒ������ʳƷ�İ�װ | |
| D�� | �������ֿ���ʳƷ�ı��ʼ� |
