题目内容
下列说法中正确的是( )
| A、工业上通过设法除去乙醇和氢氧化钠的作用生成的水来制取乙醇钠 |
| B、只使用试管和胶头滴管即可鉴别NaNO2、NaCl、AgNO3、H2SO4四种无色溶液 |
| C、将燃烧的镁条伸入混合气体,以除去CO2中的N2 |
| D、用硫酸镁和硫酸亚铁混合溶液制摩尔盐的过程:蒸发浓缩→冷却结晶→抽滤→用水洗涤2-3次 |
考点:物质的检验和鉴别的基本方法选择及应用,物质的分离、提纯和除杂
专题:实验评价题
分析:A.加入Na与水反应,促进乙醇与NaOH的反应正向移动;
B.AgNO3与其它三种物质均反应生成白色沉淀;
C.二氧化碳、氮气均与Mg反应;
D.摩尔盐在乙醇中的溶解度更小.
B.AgNO3与其它三种物质均反应生成白色沉淀;
C.二氧化碳、氮气均与Mg反应;
D.摩尔盐在乙醇中的溶解度更小.
解答:
解:A.加入Na与水反应,促进乙醇与NaOH的反应正向移动,则可通过设法除去乙醇和氢氧化钠的作用生成的水来制取乙醇钠,故A正确;
B.AgNO3与其它三种物质均反应生成白色沉淀,不能鉴别其它三种物质,故B错误;
C.二氧化碳、氮气均与Mg反应,不能除杂,将原物质反应掉,故C错误;
D.摩尔盐在乙醇中的溶解度更小,则制摩尔盐的过程:蒸发浓缩→冷却结晶→抽滤→用乙醇洗涤2-3次,故D错误;
故选A.
B.AgNO3与其它三种物质均反应生成白色沉淀,不能鉴别其它三种物质,故B错误;
C.二氧化碳、氮气均与Mg反应,不能除杂,将原物质反应掉,故C错误;
D.摩尔盐在乙醇中的溶解度更小,则制摩尔盐的过程:蒸发浓缩→冷却结晶→抽滤→用乙醇洗涤2-3次,故D错误;
故选A.
点评:本题考查物质的检验和鉴别,为高频考点,涉及混合物分离提纯、物质鉴别及除杂等,选项A为解答的难点,注意平衡移动的应用,题目难度中等.

练习册系列答案
相关题目
酸根RO3-所含电子数比硝酸根NO3-的电子数多10,则下列说法正确的是( )
| A、R原子的电子层数比N的电子层数多1 |
| B、RO3-中R的化合价与NO3-中N化合价不等 |
| C、RO3-和NO3-只能被还原,不能被氧化 |
| D、R与N为同族元素 |
根据下列各题所给出的数据,得出的结论错误的是( )
| A、同温同压下,V L CO和H2的混合气体,完全燃烧消耗O2的体积为0.5V L | ||
| B、4.2g氮气和4.8g某单质RX所含原子个数相同,且分子个数之比为1:1,则R的相对原子质量为16 | ||
C、已知某氢氧化钠溶液中Na+与H2O的个数之比为1:a,则可求出此溶液中氢氧化钠的质量分数为
| ||
| D、将98g H2SO4溶于1L水中,则所制得的H2SO4溶液的物质的量浓度为1mol/L |
已知X、Y中含有相同的元素,Z、W中也含有相同的元素,根据反应X+H2O→Y+H2;Z+H2O→W+O2 (方程式均未配平),可推断X、Y中及Z、W中相同元素的化合价的高低顺序为( )
| A、X>Y、Z>W |
| B、X<Y、Z<W |
| C、X>Y、Z<W |
| D、X<Y、Z>W |
下列说法不正确的是( )
| A、汤姆生、卢瑟福、威尔等科学家对原子结构模型的提出作出了很大贡献 |
B、海水提取单质镁的主要步骤为: |
| C、酸碱盐各物质的组成中一定都含有非金属元素 |
| D、严格地讲,“通风橱”是一种不负责任的防污染手段,因为实验产生的有害气体没有得到转化或吸收 |
如图是元素周期表短周期的一部分,Y、W的质子数之和为25.下列说法正确的是( )
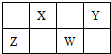

| A、非金属性:W>Z |
| B、原子半径:X<Y |
| C、Z的最高价氧化物可溶于Y的氢化物的水溶液 |
| D、Y的最高价氧化的水化物酸性强于W最高价氧化的水化物 |
常温下,0.1mol?L-1某一元酸(HA)溶液中
=1×10-8,下列叙述正确的是( )
| c(OH-) |
| c(H+) |
| A、由pH=3的HA与pH=11的NaOH溶液等体积混合,溶液中c(Na+)>c(Ac-)>c(OH-)>c(H+) |
| B、0.1mol?L-1 HA溶液与0.05mol?L-1 NaOH溶液等体积混合后所得溶液中,2c(H+)+c(HA)=c(A-)+c(OH-) |
| C、该溶液中由水电离出的c(H+)=1×10-11mol?L-1 |
| D、浓度均为0.1mol/L的HA和NaA溶液等体积混合后,若溶液呈酸性,则c(A-)>c(HA)>c(Na+)>c(H+)>c(OH-) |
日常生活中不用水而用有机溶剂(如CCl4)溶解油漆,主要考虑溶剂的( )
| A、酸碱性 | B、稳定性 |
| C、分子的极性 | D、键的极性 |
