题目内容
为进行Ⅰ项中的除杂实验(括号内为杂质),请从Ⅱ项中选出一种试剂,从Ⅲ项中选出合适的实验操作方法分离,将标号填在后面的答案栏内.
| Ⅰ除杂实验 | Ⅱ试剂 | Ⅲ操作方法 | 答案 | ||
| Ⅰ | Ⅱ | Ⅲ | |||
| ①苯(苯甲酸) | A.饱和Na2CO3溶液 B.溴水 C.NaOH溶液 D.CaO | a.蒸馏 b.分液 c.洗气 d.过滤 | ① | ||
| ②乙醇(水) | ② | ||||
| ③乙烷(乙烯) | ③ | ||||
| ④乙酸乙酯(乙酸) | ④ | ||||
考点:物质的分离、提纯的基本方法选择与应用
专题:
分析:①苯甲酸与NaOH反应后,与苯分层;
②水与CaO反应后,增大与乙醇的沸点差异;
③乙烯与溴水反应,乙烷不能;
④乙酸和碳酸钠,同时碳酸钠降低乙酸乙酯的溶解度.
②水与CaO反应后,增大与乙醇的沸点差异;
③乙烯与溴水反应,乙烷不能;
④乙酸和碳酸钠,同时碳酸钠降低乙酸乙酯的溶解度.
解答:
解:①苯甲酸与NaOH反应后,与苯分层,然后分液可分离;
②水与CaO反应后,增大与乙醇的沸点差异,然后蒸馏可分离;
③乙烯与溴水反应,乙烷不能,则选择洗气法分离;
④乙酸和碳酸钠,同时碳酸钠降低乙酸乙酯的溶解度,然后分液可分离,
故答案为:
②水与CaO反应后,增大与乙醇的沸点差异,然后蒸馏可分离;
③乙烯与溴水反应,乙烷不能,则选择洗气法分离;
④乙酸和碳酸钠,同时碳酸钠降低乙酸乙酯的溶解度,然后分液可分离,
故答案为:
| ① | C | b |
| ② | D | a |
| ③ | B | c |
| ④ | A | b |
点评:本题考查混合物的分离、提纯,为高频考点,明确物质的性质及常见的混合物的分离方法是解答本题的关键,乙醇中混有水应加生石灰为解答的难点,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
关于从碘水中分离出碘单质的实验,下列说法正确的是( )
| A、可以用酒精萃取出碘单质 |
| B、可以用CCl4萃取出碘单质,理由是CCl4密度比水大 |
| C、若用CCl4萃取出碘单质,萃取后下层液体呈紫红色 |
| D、若用CCl4萃取出碘单质,萃取后无色液体层应从分液漏斗的上口倒出 |
1.0molPCl5充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl5(g)?PCl3(g)+Cl2(g)达平衡时,PCl3(g) 为0.4mol,如果此时再加入1.0molPCl5(g),在相同条件下再达到平衡时,下列说法正确的是( )
| A、PCl5为0.6mol |
| B、PCl3大于0.8mol |
| C、再次达平衡时PCl5的体积分数比原平衡减小 |
| D、再次达平衡时PCl5的转化率比原平衡减小 |
下列说法错误的是( )
| A、常温下,若醋酸钠与醋酸的混合溶液pH=7,则C(Na+)=c(CH3COO-) |
| B、某温度下,pH=6的NaCl溶液中离子浓度的大小关系:c(Na+)=c(Cl-)>c(H+)>c(OH-) |
| C、若2a mol?L-1HCN与a mol?L-1 NaOH溶液等体积混合后所得溶液中c(Na+)>c(CN-),则混合溶液pH>7 |
| D、含0.1 mol NaHCO3和0.2molNa2CO3的混合液中:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
如图表示汽车尾气净化处理示意图:有关叙述正确的是( )
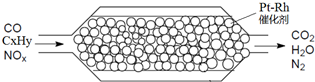

| A、NOX全部被过量CO还原为N2 |
| B、安装有该净化器的汽车可以使用含铅汽油 |
| C、催化剂涂在蜂窝状陶瓷上,可以提高反应速率 |
| D、当产生2.24L氮气时,转移的电子为4xmol |
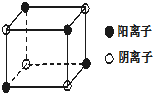 现有部分前四周期7种元素,原子序数依次增大,它们的性质或原子结构如下表:
现有部分前四周期7种元素,原子序数依次增大,它们的性质或原子结构如下表: