题目内容
[化学--选修有机化学基础]
雷诺嗪是治疗慢性心绞痛首选新药.雷诺嗪合成路线如下:
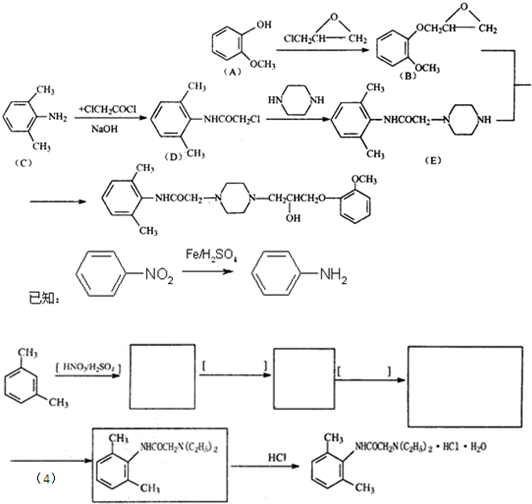
(1)雷诺嗪中含氧官能团,除酰胺键(-NHCO-)外,另两种官能团名称:
(2)写出满足下列条件A的同分异构体的数目
①能与FeCl3溶液发生显色反应;②1molA的同分异构体可与2mol NaOH反应.
(3)C→D中,加入适量NaOH的作用是:
(4)从雷诺嗪合成路线得到启示,可用间二甲苯、ClCH2COCl、(C2H5)NH(无机试剂任用)合成盐酸利多卡因,请在横线上补充反应物,在方框内补充生成物.
雷诺嗪是治疗慢性心绞痛首选新药.雷诺嗪合成路线如下:

(1)雷诺嗪中含氧官能团,除酰胺键(-NHCO-)外,另两种官能团名称:
羟基
羟基
、醚键
醚键
.(2)写出满足下列条件A的同分异构体的数目
6
6
.①能与FeCl3溶液发生显色反应;②1molA的同分异构体可与2mol NaOH反应.
(3)C→D中,加入适量NaOH的作用是:
与取代产物HCl反应,使平衡向生成D的方向移动,提高D的产率
与取代产物HCl反应,使平衡向生成D的方向移动,提高D的产率
.(4)从雷诺嗪合成路线得到启示,可用间二甲苯、ClCH2COCl、(C2H5)NH(无机试剂任用)合成盐酸利多卡因,请在横线上补充反应物,在方框内补充生成物.
分析:(1)根据雷诺嗪的结构判断含有的官能团;
(2)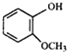 的同分异构体中,能与FeCl3溶液发生显色反应,含有酚羟基-OH,1mol可与2molNaOH反应、分子中含有2个酚羟基,故还含有1个-CH3,定2个酚羟基位置,移动-CH3,确定同分异构体数目;
的同分异构体中,能与FeCl3溶液发生显色反应,含有酚羟基-OH,1mol可与2molNaOH反应、分子中含有2个酚羟基,故还含有1个-CH3,定2个酚羟基位置,移动-CH3,确定同分异构体数目;
(3)反应中生成HCl,氢氧化钠与HCl反应,使平衡向生成D的方向移动,提高D的产率;
(4)间二甲苯发生硝化反应生成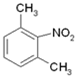 ,在Fe/HCl作用下生成
,在Fe/HCl作用下生成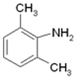 ,再ClCH2COCl作用下生成
,再ClCH2COCl作用下生成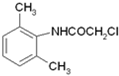 ,与(C2H5)2N生成
,与(C2H5)2N生成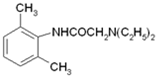 ,用HCl酸化可得盐酸利多卡因.
,用HCl酸化可得盐酸利多卡因.
(2)
 的同分异构体中,能与FeCl3溶液发生显色反应,含有酚羟基-OH,1mol可与2molNaOH反应、分子中含有2个酚羟基,故还含有1个-CH3,定2个酚羟基位置,移动-CH3,确定同分异构体数目;
的同分异构体中,能与FeCl3溶液发生显色反应,含有酚羟基-OH,1mol可与2molNaOH反应、分子中含有2个酚羟基,故还含有1个-CH3,定2个酚羟基位置,移动-CH3,确定同分异构体数目;(3)反应中生成HCl,氢氧化钠与HCl反应,使平衡向生成D的方向移动,提高D的产率;
(4)间二甲苯发生硝化反应生成
 ,在Fe/HCl作用下生成
,在Fe/HCl作用下生成 ,再ClCH2COCl作用下生成
,再ClCH2COCl作用下生成 ,与(C2H5)2N生成
,与(C2H5)2N生成 ,用HCl酸化可得盐酸利多卡因.
,用HCl酸化可得盐酸利多卡因.解答:解:(1)由雷诺嗪的结构可知,雷诺嗪中含氧官能团,除酰胺键(-NHCO-)外,另两种官能团为羟基、醚键,
故答案为:羟基、醚键;
(2) 的同分异构体中,能与FeCl3溶液发生显色反应,含有酚羟基-OH,1mol可与2molNaOH反应、分子中含有2个酚羟基,故还含有1个-CH3,定2个酚羟基位置,移动-CH3,若2个-OH相邻,-CH3有2种位置,若2个-OH相间,-CH3有3种位置,若2个-OH对,-CH3有1种位置,故符合条件的同分异构体有2+3+1=6种,
的同分异构体中,能与FeCl3溶液发生显色反应,含有酚羟基-OH,1mol可与2molNaOH反应、分子中含有2个酚羟基,故还含有1个-CH3,定2个酚羟基位置,移动-CH3,若2个-OH相邻,-CH3有2种位置,若2个-OH相间,-CH3有3种位置,若2个-OH对,-CH3有1种位置,故符合条件的同分异构体有2+3+1=6种,
故答案为:6;
(3)反应中生成HCl,氢氧化钠与HCl反应,使平衡向生成D的方向移动,提高D的产率,
故答案为:与取代产物HCl反应,使平衡向生成D的方向移动,提高D的产率;
(4)盐酸利多卡因的合成路线图为: ,
,
故答案为: ,Fe/HCl,
,Fe/HCl, ,ClCH2COCl,
,ClCH2COCl, .
.
故答案为:羟基、醚键;
(2)
 的同分异构体中,能与FeCl3溶液发生显色反应,含有酚羟基-OH,1mol可与2molNaOH反应、分子中含有2个酚羟基,故还含有1个-CH3,定2个酚羟基位置,移动-CH3,若2个-OH相邻,-CH3有2种位置,若2个-OH相间,-CH3有3种位置,若2个-OH对,-CH3有1种位置,故符合条件的同分异构体有2+3+1=6种,
的同分异构体中,能与FeCl3溶液发生显色反应,含有酚羟基-OH,1mol可与2molNaOH反应、分子中含有2个酚羟基,故还含有1个-CH3,定2个酚羟基位置,移动-CH3,若2个-OH相邻,-CH3有2种位置,若2个-OH相间,-CH3有3种位置,若2个-OH对,-CH3有1种位置,故符合条件的同分异构体有2+3+1=6种,故答案为:6;
(3)反应中生成HCl,氢氧化钠与HCl反应,使平衡向生成D的方向移动,提高D的产率,
故答案为:与取代产物HCl反应,使平衡向生成D的方向移动,提高D的产率;
(4)盐酸利多卡因的合成路线图为:
 ,
,故答案为:
 ,Fe/HCl,
,Fe/HCl, ,ClCH2COCl,
,ClCH2COCl, .
.点评:本题考查有机物的推断与合成、官能团、同分异构体书写等,难度中等,注意根据题目中转化关系与反应信息进行(4)中合成路线的设计.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目




 [化学选修3:物质结构与性质]
[化学选修3:物质结构与性质]