题目内容
下列各组物质混合,加热蒸干,并经充分灼烧,得到的是混合物的是( )
| A、0.2mol/L NaHCO3溶液与0.1mol/LNaOH溶液等体积混合 |
| B、向400mL、2mol/L的NaOH溶液中通入6.72LCO2(标况) |
| C、在100mL1mol/LNH4Cl溶液中,投入0.05molNa2O2 |
| D、在20mL0.01mol/LCa(HCO3)2溶液中,投入0.2gCaCO3 |
考点:化学方程式的有关计算
专题:计算题
分析:A.NaHCO3过量,反应后为Na2CO3、NaHCO3混合溶液,加热蒸干,灼烧,碳酸氢钠分解生成碳酸钠;
B.NaOH为0.8mol,二氧化碳为0.3mol,二者物质的量之比为8:3,大于2:1,反应生成碳酸钠,且氢氧化钠有剩余;
C.0.05molNa2O2与水反应生成0.1molNaOH,NH4Cl为0.1mol,氢氧化钠与氯化铵恰好反应生成氯化钠与一水合氨,加热得到氯化钠;
D.加热蒸干,灼烧,碳酸氢钙、碳酸钙分解得到氧化钙.
B.NaOH为0.8mol,二氧化碳为0.3mol,二者物质的量之比为8:3,大于2:1,反应生成碳酸钠,且氢氧化钠有剩余;
C.0.05molNa2O2与水反应生成0.1molNaOH,NH4Cl为0.1mol,氢氧化钠与氯化铵恰好反应生成氯化钠与一水合氨,加热得到氯化钠;
D.加热蒸干,灼烧,碳酸氢钙、碳酸钙分解得到氧化钙.
解答:
解:A.发生反应:NaHCO3+NaOH=Na2CO3+H2O,NaHCO3过量,反应后为Na2CO3、NaHCO3混合溶液,加热蒸干,灼烧,碳酸氢钠分解生成碳酸钠,最终得到碳酸钠,故A不符合;
B.NaOH为0.8mol,二氧化碳为0.3mol,二者物质的量之比为8:3,大于2:1,反应生成碳酸钠,且氢氧化钠有剩余,最终为碳酸钠、氢氧化钠化合物,故B符合;
C.0.05molNa2O2与水反应生成0.1molNaOH,NH4Cl为0.1mol,氢氧化钠与氯化铵恰好反应生成氯化钠与一水合氨,加热得到固体为氯化钠,故C不符合;
D.加热蒸干,灼烧,碳酸氢钙、碳酸钙分解得到氧化钙,故D不符合,
故选B.
B.NaOH为0.8mol,二氧化碳为0.3mol,二者物质的量之比为8:3,大于2:1,反应生成碳酸钠,且氢氧化钠有剩余,最终为碳酸钠、氢氧化钠化合物,故B符合;
C.0.05molNa2O2与水反应生成0.1molNaOH,NH4Cl为0.1mol,氢氧化钠与氯化铵恰好反应生成氯化钠与一水合氨,加热得到固体为氯化钠,故C不符合;
D.加热蒸干,灼烧,碳酸氢钙、碳酸钙分解得到氧化钙,故D不符合,
故选B.
点评:本题考查化学方程式计算、元素化合物性质等,难度不大,明确发生的反应是关键,注意对基础知识的理解掌握.

练习册系列答案
相关题目
下列实验过程中会先产生白色沉淀后沉淀又溶解的是( )
| A、向AlCl3溶液中滴加氨水至过量 |
| B、向Ba(NO3)2溶液通入SO2至过量 |
| C、向Ba(0H)2溶液通入CO2至过量 |
| D、向新制Fe(OH)3胶体中滴加稀硫酸至过量 |
含有砒霜(As2O3)的试样和锌、盐酸混合反应,生成的砷化氢(AsH3)在热玻璃管中完全分解成单质砷和氢气.若砷的质量为1.50g,则( )
| A、被氧化的砒霜为1.98 g |
| B、分解产生的氢气为672 mL |
| C、和砒霜反应的锌为3.90 g |
| D、转移的电子总数为0.06NA |
以碳原子为中心与两个氯原子及两个碘原子相结合形成CCl2I2分子,以下判断正确的是( )
| A、CCl2I2分子是非极性分子 |
| B、CCl2I2分子含有π键 |
| C、CCl2I2分子是手性分子 |
| D、CCl2I2的沸点高于CCl4 |
通常把原子总数和价电子总数相同的分子或离子称为等电子体.等电子体具有相似的化学结构,则下列有关说法中正确的是( )
| A、CH4和NH4+是等电子体,化学键类型完全相同 |
| B、NO3-和CO32-是等电子体,均为平面正三角形结构 |
| C、H3O+和PCl3是等电子体,均为三角锥形结构 |
| D、SO2和O3是等电子体,SO2和O3具有相同的化学性质 |
短周期元素M、W、X、Y、Z的原子序数依次增大,且M、W、X、Y+、Z2-的电子数与其电子层数的比值依次为1、3、4、5、6(不考虑零族元素).下列关于这些元素的叙述正确的是( )
| A、X分别和其它四种元素均可形成至少2种化合物 |
| B、X、Y、Z离子半径依次增大 |
| C、M、X、Z三种元素组成的化合物含有离子键 |
| D、W、X、Z对应气态氢化物稳定性依次增强 |
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示.下列说法正确的是( )
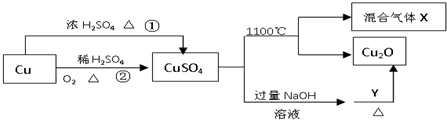

| A、相对于途径①,途径②更好地体现了绿色化学思想 |
| B、Y可以是蔗糖溶液 |
| C、CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 |
| D、将CuSO4溶液蒸发、利用余热蒸干,可制得胆矾晶体 |