题目内容
19.为使以面粉为原料的面包松软可口,通常用碳酸氢钠作发泡剂,其原因是( )①热稳定性差
②增加甜味
③产生二氧化碳
④提供钠离子.
| A. | ②③ | B. | ①③ | C. | ①④ | D. | ③④ |
分析 碳酸氢钠不稳定,加热易分解生成二氧化碳气体,可使面包疏松多孔而导致松软可口,以此解答.
解答 解:由2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑可知,碳酸氢钠极易受热分解,生成碳酸钠,水和二氧化碳,生成的气体在面团里形成大量气泡,使得面包变得松软.
故选B.
点评 本题考查碳酸氢钠知识,侧重于化学与生活的考查,为高频考点,有利于培养学生的良好科学素养和题给学生的学习积极性,难度不大,注意相关基础知识的积累.

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
9.下列说法不正确的是( )
| A. | 在氧化还原反应中,氧化剂与还原剂不一定是两种不同的反应物 | |
| B. | 在氧化还原反应中,生成物不一定是氧化产物或还原产物 | |
| C. | 元素由化合态转化为游离态时,该元素一定被还原 | |
| D. | 有单质参加的反应不一定属于氧化还原反应 |
14.高铁电池是一种可逆电池,该电池能长时间保持稳定的放电电压.高铁电池总反应为3Zn+2K2Fe04+8H20?3Zn(OH)2+2Fe(OH)3+4KOH.下列判断不正确的是( )
| A. | 放电时,负极反应为2n-2e-+20H一═Zn(OH)2 | |
| B. | 充电时,阴极pH增大 | |
| C. | 放电时,若有6mol电子转移,则正极有10 mol OH一移向负极 | |
| D. | 充电时,阳极反应为Fe(OH)3+50H一+3e一=Fe042-+4H20 |
11.在热的稀H2SO4溶液中溶解了45.6g FeSO4,当加入100mL 1mol/L KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3也反应完全,并有NxOy气体逸出:□FeSO4+□KNO3+□H2SO4→K2SO4+□Fe2(SO4)3+□NxOy+□H2O据此推算出x、y的值分别为( )
| A. | 1、2 | B. | 1、1 | C. | 2、1 | D. | 2、3 |
8.在0.1mol/L的CH3COOH溶液中存在如下电离平衡CH3COOH?CH3COO-+H+对于该平衡,下列叙述正确的是( )
| A. | 加入少量NaOH固体,平衡向正反应方向移动 | |
| B. | 加水,反应速率增大,平衡向逆反应方向移动 | |
| C. | 滴加少量0.1mol/LHCl溶液,溶液中C(H+)减少 | |
| D. | 加入少量CH3COONa固体,平衡向正反应方向移动 |
9.某有机物在氧气中充分燃烧,生成的CO2和H2O的物质的量之比为1:2,则( )
| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:2 | ||
| C. | 有机物一定是CH4 | D. | 有机物可能是CH4O |
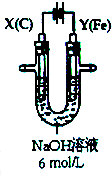 用如图所示装置进行实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.
用如图所示装置进行实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.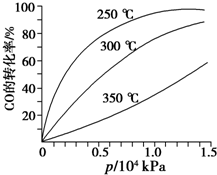 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.