题目内容
正确掌握好化学用语是学好化学的基础,下列有关表述正确的是( )
A、HClO的电子式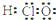 |
B、比例模型 :可以表示CH4,也可以表示CCl4 :可以表示CH4,也可以表示CCl4 |
| C、乙烯的结构简式:CH2CH2 |
| D、碳酸氢根电离:HCO3-+H2O?H3O++CO32- |
考点:电子式、化学式或化学符号及名称的综合,电离方程式的书写
专题:
分析:A.根据稳定结构分析,次氯酸分子中O原子分别与H原子、Cl原子之间形成1对共用电子对;
B.四氯化碳分子中,碳原子半径小于氯原子,比例模型中Cl原子的相对体积应该大于C原子;
C.乙烯分子中含有碳碳双键,结构简式中必须标出其含有的官能团结构;
D.碳酸氢根离子在溶液中电离出氢离子和碳酸根离子.
B.四氯化碳分子中,碳原子半径小于氯原子,比例模型中Cl原子的相对体积应该大于C原子;
C.乙烯分子中含有碳碳双键,结构简式中必须标出其含有的官能团结构;
D.碳酸氢根离子在溶液中电离出氢离子和碳酸根离子.
解答:
解:A.根据稳定结构分析,次氯酸分子中O原子分别与H原子、Cl原子之间形成1对共用电子对,其电子式为 ,故A错误;
,故A错误;
B. 可以表示甲烷分子的比例模型,但是不能表示四氯化碳,因为四氯化碳分子中碳原子半径小于氯原子,四氯化碳的比例模型为:
可以表示甲烷分子的比例模型,但是不能表示四氯化碳,因为四氯化碳分子中碳原子半径小于氯原子,四氯化碳的比例模型为: ,故B错误;
,故B错误;
C.乙烯的结构简式中需要标出其含有的碳碳双键,乙烯正确的结构简式为:CH2=CH2,故C错误;
D.碳酸氢根离子电离出氢离子和碳酸根离子,其电离方程式为:HCO3-+H2O?H3O++CO32-,故D正确;
故选D.
 ,故A错误;
,故A错误;B.
 可以表示甲烷分子的比例模型,但是不能表示四氯化碳,因为四氯化碳分子中碳原子半径小于氯原子,四氯化碳的比例模型为:
可以表示甲烷分子的比例模型,但是不能表示四氯化碳,因为四氯化碳分子中碳原子半径小于氯原子,四氯化碳的比例模型为: ,故B错误;
,故B错误;C.乙烯的结构简式中需要标出其含有的碳碳双键,乙烯正确的结构简式为:CH2=CH2,故C错误;
D.碳酸氢根离子电离出氢离子和碳酸根离子,其电离方程式为:HCO3-+H2O?H3O++CO32-,故D正确;
故选D.
点评:本题考查了常见化学用语的表示方法判断,难度中等,注意掌握常见化学用语的概念及书写原则,A选项为易错点,学生容易受次氯酸的化学式影响;还要注意结构简式中碳碳双键、碳碳三键不能省略.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
等质量的铝分别与足量的稀盐酸和氢氧化钠溶液反应,两个反应放出的气体在相同状况下体积比为( )
| A、3:1 | B、2:1 |
| C、1:1 | D、1:3 |
下列物质中所含分子个数最多的是( )
| A、2.7g H2O |
| B、2.24L CO(标准状况下) |
| C、6.02×1022个HCl分子 |
| D、4.9g H2SO4 |
某氯原子的质量为a g,12C原子的质量为b g.用NA表示阿伏加德罗常数.下列说法中不正确的是( )
A、则该氯原子构成氯分子的相对分子质量为
| ||
B、m g该氯原子的物质的量为
| ||
C、n g该氯原子所含的电子为
| ||
| D、1 mol该氯原子的质量为aNA g |
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则( )
| A、甲的分子数比乙的分子数多 |
| B、甲的体积比乙大 |
| C、两气体的气体摩尔体积相同 |
| D、甲的相对分子质量比乙的相对分子质量小 |
下列溶液中的Cl-数目与50mL 1mol/L的AlCl3溶液中Cl-数目相等的是( )
| A、150mL 1mol/L的NaCl |
| B、75mL 1mol/L的FeCl3 |
| C、150mL 3mol/L的KCl |
| D、75mL 2mol/L的CaCl2 |