��Ŀ����
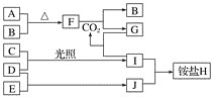
����Ŀ����A��B��C��D��E��F6�ֶ�����Ԫ�أ�GΪ����Ԫ�أ���֪���ڵ�A��B��C��D 4��Ԫ��ԭ�Ӻ����56�����ӣ������ڱ��е�λ����ͼ��ʾ��1molE���������������ã��ڱ�״�����ܲ���33.6LH2��E���ʷ�ĩ��G�������ﳣ����Ұ�⺸�Ӹֹ죻F�Ƕ���������õĽ���Ԫ�ء���ش��������⣺
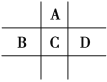
��1��Ԫ��D��G�����Ʒֱ�Ϊ��__��
��2��D�ĵ�����C����̬�⻯�ﷴӦ����ʽΪ___��
��3��C��E��A�ļ����Ӱ뾶��__��__��__��B��C��D������������Ӧ��ˮ���������ǿ��˳��Ϊ___(�û�ѧʽ��ʾ)��
��4����D��E�γɵĻ������ˮ��Һ�еμӹ����ռ���Һ�����ӷ���ʽΪ__��
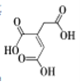
��5���õ���ʽ��ʾF��C�γɻ�����Ĺ���___��
��6��G�ĵ��������ˮ������Ӧ�ķ���ʽ___��
��7������Ԫ�������ڱ��еķֲ���ͼ��ʾ������Ϊ����Ԫ����ǽ���Ԫ�صķֽ��ߣ�������˵������ȷ����___��
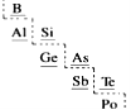
A��Bֻ�ܵõ��ӣ�����ʧ���� B��ԭ�Ӱ뾶Ge��Si
C��As�����뵼����� D��Po���ڵ������ڵ�VIA��
���𰸡��� �� Cl2+H2S=2HCl+S�� S2�� O2�� Al3�� HClO4��H2SO4��H3PO4 Al3+��4OH-=AlO2-��2H2O ![]() 3Fe��4H2O
3Fe��4H2O![]() Fe3O4+4H2 A
Fe3O4+4H2 A
��������
��C��ԭ������Ϊx����AΪx-8��BΪx-1��CΪx+1��A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ�����x+x-8+x-1+x+1=56��x=16������CΪSԪ�أ�AΪOԪ�أ�BΪPԪ�أ�DΪClԪ�أ�1molE���������������ã��ڱ�״�����ܲ���33.6LH2����֪E�Ļ��ϼ�Ϊ+3�ۣ�ӦΪAlԪ�أ�E���ʷ�ĩ��G�������ﳣ����Ұ�⺸�Ӹֹ죬GΪFe��F�Ƕ���������õĽ���Ԫ�أ�FΪNa������Ԫ�������ɵĵݱ���ɱȽ�ԭ�Ӱ뾶�Լ�Ԫ�صķǽ�����ǿ�������Ԫ�ض�Ӧ�ĵ��ʡ�����������ʽ����⡣
��1�����ݷ�����Ԫ��DΪ�ȣ�Ԫ��GΪ����
��2��D�ĵ�����C����̬�⻯�ﷴӦ�����������ⷴӦ�������Ȼ�������ʣ���Ӧ����ʽΪCl2+H2S=2HCl+S����
��3�����ݵ��Ӳ���Խ�࣬�뾶Խ������ͬ�ṹ�����ӣ�ԭ������ԽС�����Ӱ뾶Խ�������Ӱ뾶ΪS2-��O2-��Al3����Ԫ�صķǽ�����Խǿ����Ӧ������������Ӧˮ���������Խǿ������HClO4��H2SO4��H3PO4��
��4��D��E�γɵĻ�����ΪAlCl3��ˮ��Һ�е�������ռ���Һ����ƫ�����ƺ�ˮ�����ӷ�ӦΪAl3++4OH--=AlO2-+2H2O��
��5���ƺ������γ��Ȼ��ƵĹ����У���ԭ��ʧȥһ�������γ������ӣ���ԭ�ӵõ�һ�������γ������ӣ�֮���������Ȼ��ƣ�����ʽ��ʾΪ![]()
��6��GΪ���������������ˮ������Ӧ������������������������Ӧ����ʽΪ3Fe��4H2O![]() Fe3O4+4H2��
Fe3O4+4H2��
��7��A��B����ʧ���ӣ�H3BO3��B��+3�ۣ���Aѡ�����
B��ͬһ����Խ����ԭ�Ӱ뾶Խ��ԭ�Ӱ뾶Ge��Si��Bѡ����ȷ��
C��As��Si��ѧ���ʽ������Ҳ�����뵼����ϣ���Cѡ����ȷ��
D��Po�����ڱ��д��ڵ������ڵ�VIA�壬��Dѡ����ȷ��
�ʴ�ѡA

����Ŀ����֪��ӦX(g)��Y(g)![]() R(g)��Q(g)��ƽ�ⳣ�����¶ȵĹ�ϵ�����ʾ��830 ��ʱ����һ��2 L���ܱ������г���0.2 mol X��0.8 mol Y����Ӧ��ʼ4 s��v(X)��0.005 mol/(L��s)������˵����ȷ����
R(g)��Q(g)��ƽ�ⳣ�����¶ȵĹ�ϵ�����ʾ��830 ��ʱ����һ��2 L���ܱ������г���0.2 mol X��0.8 mol Y����Ӧ��ʼ4 s��v(X)��0.005 mol/(L��s)������˵����ȷ����
�¶�/�� | 700 | 800 | 830 | 1 000 | 1 200 |
ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
A. 4 sʱ������c(Y)��0.76 mol/L
B. 830 ����ƽ��ʱ��X��ת����Ϊ80%
C. ��Ӧ��ƽ��������¶ȣ�ƽ�������ƶ�
D. 1 200 ��ʱ��ӦR(g)��Q(g) ![]() X(g)��Y(g)��ƽ�ⳣ��K��0.4
X(g)��Y(g)��ƽ�ⳣ��K��0.4
����Ŀ��Ԫ�����ڱ���ѧϰ��ѧ����Ҫ���ߣ���������������Ϣ���ɡ��±����������ֶ�����Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼ�(��֪���ԭ�Ӱ뾶Ϊ0.089 nm)��
Ԫ�ش��� | A | B | C | D | E |
ԭ�Ӱ뾶/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
��Ҫ���ϼ� | ��2 | ��3 | ��6����2 | ��1 | ��2 |
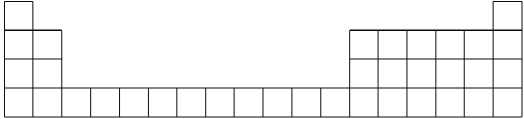
(1)��Ԫ�ش��ű�����������ڱ�������Ӧ��λ��(����Ϊ���ڱ���һ����)_________��
(2)����A��ԭ�ӽṹʾ��ͼ_________��
(3)BԪ�ش������ڱ��е�________���ڣ�________�塣
(4)EԪ�ش������ڱ��е�________���ڣ�________�塣
(5)C��D�ļ����ӵİ뾶�ɴ�С˳��Ϊ________(�����ӷ��ű�ʾ)��
(6)��������Ԫ�ص�����������Ӧ��ˮ������������ǿ����__________(�ѧʽ)��
(7)C��E�γɵĻ�����Ϊ________(�ѧʽ)��
(8)д��B���ʺ�����������Һ��Ӧ�ķ���ʽ__________д��B������������Ӧˮ���������������Һ��Ӧ�����ӷ���ʽ��________