题目内容
用表示阿伏加德罗常数的值.下列叙述中不正确的是( )
| A、16.9 g过氧化钡(BaO2)加入足量H2O中转移电子数目为0.1NA |
| B、常温常压下,28 g乙烯含有的电子数为16NA |
| C、标准状况下,ag某气体舍分子数为b,则cg该气体的体积为bc/a L |
| D、1 mol丙烷分子中含有的共用电子对数为8NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.依据反应2BaO2+2H2O═2Ba(OH)2+O2↑判断解答;
B.1个乙烯分子含有16个电子;
C.先计算该气体的摩尔质量,然后计算Cg气体的物质的量和标况下气体的体积;
D.1个丙烷分子中含有8个C-H键和2个C-C键,10对共用电子对.
B.1个乙烯分子含有16个电子;
C.先计算该气体的摩尔质量,然后计算Cg气体的物质的量和标况下气体的体积;
D.1个丙烷分子中含有8个C-H键和2个C-C键,10对共用电子对.
解答:
解:A.依据反应2BaO2+2H2O═2Ba(OH)2+O2↑,过氧化钡既做氧化剂又做还原剂,2mol过氧化钡与水反应转移2mol电子,16.9 g过氧化钡的物质的量为0.1mol,与水反应转移0.1mol电子,故A正确;
B.1个乙烯分子含有16个电子,28 g乙烯的物质的量为1mol,含有电子数为16NA,故B正确;
C.ag某气体舍分子数为b,则该气体的摩尔质量=
,cg该气体标况下的体积=(c÷
)×22.4L/mol,故C错误;
D.1个丙烷分子中含有8个C-H键和2个C-C键,10对共用电子对,1 mol丙烷分子中含有的共用电子对数为10NA,故D错误;
故选:CD.
B.1个乙烯分子含有16个电子,28 g乙烯的物质的量为1mol,含有电子数为16NA,故B正确;
C.ag某气体舍分子数为b,则该气体的摩尔质量=
| aNA |
| b |
| aNA |
| b |
D.1个丙烷分子中含有8个C-H键和2个C-C键,10对共用电子对,1 mol丙烷分子中含有的共用电子对数为10NA,故D错误;
故选:CD.
点评:本题考查阿伏加德罗常数的应用,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,注意有机物乙烯、丙烷的结构,题目难度不大.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
下列关于硫化氢或氢硫酸的描述,正确的是( )
| A、氢硫酸因含-2价的硫,所以只有还原性 |
| B、硫化氢气体通入硫酸亚铁中有黑色沉淀生成 |
| C、实验室制取硫酸氢时,可以用稀盐酸或稀硫酸,但不能用浓硫酸或硝酸 |
| D、氢硫酸溶液中加入镁粉会有氢气产生 |
下列关于有机物的表述正确的是( )
| A、油脂可水解生成丙三醇 |
| B、乙醇经还原可生成乙醛 |
| C、乙烯与苯均可使酸性高锰酸钾溶液褪色 |
| D、淀粉、蛋白质完全水解的产物互为同分异构体 |
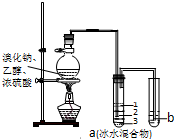 实验室制取少量溴乙烷的装置如图所示,将生成物导入盛有冰水混合物的试管a中,实验结束发现试管a中的物质分为三层.对该实验的分析错误的是( )
实验室制取少量溴乙烷的装置如图所示,将生成物导入盛有冰水混合物的试管a中,实验结束发现试管a中的物质分为三层.对该实验的分析错误的是( )| A、烧瓶中除发生取代反应可能发生消去反应、氧化还原反应等 |
| B、产物在a中第一层 |
| C、a中有产物和水还含HBr、CH3CH2OH等 |
| D、b中盛放的酸性KMnO4溶液会褪色 |
芳炔类大环化合物是新兴的一种富碳共轭大环状分子.苯乙炔( )可用于合成一系列芳炔类大环化合物,其结构如下.有关叙述正确的是( )
)可用于合成一系列芳炔类大环化合物,其结构如下.有关叙述正确的是( )

 )可用于合成一系列芳炔类大环化合物,其结构如下.有关叙述正确的是( )
)可用于合成一系列芳炔类大环化合物,其结构如下.有关叙述正确的是( )
| A、上述四种物质属于苯乙炔的同系物 |
| B、第一种物质的分子式为C18H12 |
| C、它们可通过苯乙炔的加成反应获得 |
| D、该系列化合物的含碳量均相同 |


 ,请回答
,请回答


