题目内容
某含氧有机化合物,它的相对分子质量为88.0,含C的质量分数为68.2%,含H的质量分数为13.6%,经红外光谱测定含有一个羟基,核磁共振氢谱显示该分子中有3个甲基.则其结构简式为( )
A、 |
B、 |
| C、CH3CH2CH2CH2CH2OH |
| D、CH3CH2CH2OCH2CH3 |
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:根据该有机物的相对分子量、碳元素和氢元素的质量分数计算出分子中含有的C、H原子数目,再根据相对分子质量计算出分子中含有的O的足量及数目,从而确定该有机物分子式;再根据含有1个羟基、3个甲基确定其结构简式.
解答:
解:该有机物中含有碳原子数目为:N(C)=
≈5,
含有氢原子数目为:N(H)=
≈12,
该有机物分子中含有氧原子数为:N(O)=
=1,
该有机物分子式为:C5H12O,所以B错误;
经红外光谱测定含有一个羟基,则选项D错误;
核磁共振氢谱显示该分子中有3个甲基,则选项C错误,选项A正确;
故选A.
| 88×68.2% |
| 12 |
含有氢原子数目为:N(H)=
| 88×13.6% |
| 1 |
该有机物分子中含有氧原子数为:N(O)=
| 88-12×5-1×12 |
| 16 |
该有机物分子式为:C5H12O,所以B错误;
经红外光谱测定含有一个羟基,则选项D错误;
核磁共振氢谱显示该分子中有3个甲基,则选项C错误,选项A正确;
故选A.
点评:本题考查了常见有机物分子式、结构简式的确定,题目难度中等,注意掌握常见有机物结构与性质,能够利用质量守恒定律确定有机物分子式、根据含有的官能团确定有机物结构,试题有利于培养学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案
相关题目
关于下列图示的说法不正确的是( )
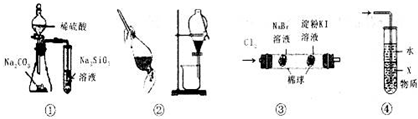

| A、图①所示实验,能比较硫、碳、硅三种元素的非金属性强弱 |
| B、装置②可用于从溴水中提取单质溴 |
| C、装置③中,左边棉花变为橙色,右边棉花变为蓝色,证明氧化性:Cl2>Br2>I2 |
| D、装置④中,X若为CCl4,可用吸收NH3或HCl,并防止倒吸 |
控制适当的条件,将反应Fe3++Ag═Fe2++Ag+设计成如图所示的原电池.下列判断正确的是( )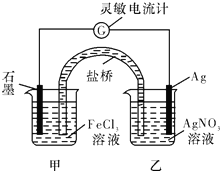

| A、反应开始时,石墨棒作阳极,银棒作阴极 |
| B、灵敏电流计的读数由小变大,再变小 |
| C、反应达化学平衡时,电流计读数最大 |
| D、反应达化学平衡时,在乙烧杯中滴入一定量的NaCl溶液,电流计指针又偏转 |
下列离子方程式不正确的是( )
| A、Na2CO3溶液与足量盐酸反应:CO32-+2H+═CO2↑+H2O |
| B、FeCl2溶液和Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
| C、钠与水反应:Na+H2O═Na++OH-+H2↑ |
| D、NaHCO3溶液与NaOH溶液:HCO3-+OH-═CO32-+H2O |
下列说法正确的是( )
| A、实验室里需要480 mL 2.0 mol?L-1的氢氧化钠溶液,配制溶液时先称量氢氧化钠固体38.4 g,然后再按照溶解、冷却、洗涤、定容、摇匀的步骤进行操作 |
| B、用标准盐酸滴定NaOH溶液测其浓度时,酸式滴定管用蒸馏水洗涤后,没用标准盐酸润洗,直接装标准盐酸滴定,所测的碱液浓度偏低 |
| C、蒸发硫酸铜溶液时蒸发皿放在石棉网上加热,并用坩埚钳夹取蒸发皿 |
| D、向氧氧化铁胶体中逐滴加入稀硫酸,先出现红褐色沉淀,继续滴加硫酸,沉淀溶解得到黄色溶液 |
对下列有关实验操作和事实解释不正确的是( )
| A、氯水和SO2使品红溶液褪色及SO2可使酸性高锰酸钾溶液褪色的原理不同 |
| B、向某溶液中加入氯化钡溶液生成白色沉淀,再加稀硝酸,白色沉淀不消失该原溶液一定含有SO42- |
| C、用KSCN溶液鉴别FeCl2溶液、FeCl3溶液 |
| D、用氢氟酸雕刻玻璃,是由于氢氟酸能与二氧化硅反应 |




 (1)硫酸是重要的化工材料,二氧化硫生成三氧化硫是工业制硫酸的重要反应之一.
(1)硫酸是重要的化工材料,二氧化硫生成三氧化硫是工业制硫酸的重要反应之一.