题目内容
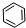
 如图表示A--E五种物质的相互转化关系,其中A为淡黄色粉末,C为单质,D为离子化合物.
如图表示A--E五种物质的相互转化关系,其中A为淡黄色粉末,C为单质,D为离子化合物.(1)推断A为
(2)写出②、③的化学方程式:②
(3)请写出过量的E和Ca(HCO3)2溶液反应的离子方程式:
(4)将C投入足量的FeCl3的水溶液中,写出发生的总反应的离子方程式.
考点:无机物的推断,钠的重要化合物
专题:推断题,几种重要的金属及其化合物
分析:A为淡黄色粉末,能和CO2、H2O反应,则A是Na2O2,B是Na2CO3、E是NaOH,C为单质,C能和水反应,则C是Na,C和氯气反应生成氯化钠,D为离子化合物,则D是NaCl,再结合物质之间的反应分析解答.
解答:
解:A为淡黄色粉末,能和CO2、H2O反应,则A是Na2O2,B是Na2CO3、E是NaOH,C为单质,C能和水反应,则C是Na,C和氯气反应生成氯化钠,D为离子化合物,则D是NaCl,
(1)通过以上分析知,A是Na2O2、B是Na2CO3、C是Na、D是NaCl,
故答案为:Na2O2;Na2CO3;Na;NaCl;
(2)过氧化钠和水反应生成氢氧化钠和氧气,反应方程式为2Na2O2+2H2O═4NaOH+O2↑,过氧化钠和二氧化碳反应生成碳酸钠和氧气,反应方程式为:2Na2O2+2CO2═2Na2CO3+O2,故答案为:2Na2O2+2H2O═4NaOH+O2↑;2Na2O2+2CO2═2Na2CO3+O2;
(3)过量的NaOH溶液和碳酸氢钙溶液反应生成碳酸钙、碳酸钠和水,离子方程式为2OH-+Ca2++2HCO3-=CaCO3↓+CO32-+2H2O,
故答案为:2OH-+Ca2++2HCO3-=CaCO3↓+CO32-+2H2O;
(4)钠先和水反应生成NaOH,NaOH再和氯化铁发生复分解反应,所以总的离子方程式为6Na+6H2O+2Fe3+=6Na++2Fe(OH)3↓+3H2↑,
故答案为:6Na+6H2O+2Fe3+=6Na++2Fe(OH)3↓+3H2↑.
(1)通过以上分析知,A是Na2O2、B是Na2CO3、C是Na、D是NaCl,
故答案为:Na2O2;Na2CO3;Na;NaCl;
(2)过氧化钠和水反应生成氢氧化钠和氧气,反应方程式为2Na2O2+2H2O═4NaOH+O2↑,过氧化钠和二氧化碳反应生成碳酸钠和氧气,反应方程式为:2Na2O2+2CO2═2Na2CO3+O2,故答案为:2Na2O2+2H2O═4NaOH+O2↑;2Na2O2+2CO2═2Na2CO3+O2;
(3)过量的NaOH溶液和碳酸氢钙溶液反应生成碳酸钙、碳酸钠和水,离子方程式为2OH-+Ca2++2HCO3-=CaCO3↓+CO32-+2H2O,
故答案为:2OH-+Ca2++2HCO3-=CaCO3↓+CO32-+2H2O;
(4)钠先和水反应生成NaOH,NaOH再和氯化铁发生复分解反应,所以总的离子方程式为6Na+6H2O+2Fe3+=6Na++2Fe(OH)3↓+3H2↑,
故答案为:6Na+6H2O+2Fe3+=6Na++2Fe(OH)3↓+3H2↑.
点评:本题以钠及其化合物为载体考查了物质推断,以A的颜色及发生的反应为突破口采用正逆结合的方法进行推断,明确物质的性质是解本题关键,再结合物质之间发生的反应解答,难点是离子方程式的书写,有的反应还与反应物的量有关,题目难度中等.

练习册系列答案
相关题目
下列化学用语的理解正确的是( )
A、2-丁醇的结构简式: |
B、电子式 :可以表示羟基,也可以表示氢氧根离子 :可以表示羟基,也可以表示氢氧根离子 |
C、比例模型  :可以表示甲烷分子,也可以表示四氯化碳分子 :可以表示甲烷分子,也可以表示四氯化碳分子 |
D、聚丙烯的结构简式: |
黑火药爆炸时发生:S+2KNO3+3C=K2S+N2↑+3CO2↑,其中被还原的物质是( )
| A、S和KNO3 |
| B、C 和S |
| C、KNO3 |
| D、C 和KNO3 |
不能用Ca2++CO32-=CaCO3↓ 表示离子反应的是( )
| A、CO2通入澄清的石灰水中 |
| B、氯化钙溶液中加入碳酸钾溶液 |
| C、澄清的石灰水与纯碱溶液混合 |
| D、碳酸铵溶液中加入硝酸钙溶液 |
 、④HCHO其中碳原子采取sp2杂化的分子有
、④HCHO其中碳原子采取sp2杂化的分子有