题目内容
ⅰ、已知A是气态烃,完全燃烧时产生的CO2和H2O 的物质的量之比为1:1,A的相对分子质量小于30,在如图1变化中,F为高分子化合物,C中含有-CHO,E有水果的香味(反应条件未写出)

(1)B中所含官能团名称 E 物质的名称
(2)反应①类型为
(3)写出下列反应的化学方程式(注明反应条件)
①
②
③
ⅱ、一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6g,若其中水的质量为10.8g,则CO的质量为 g.
ⅲ某课外活动小组利用如图2装置进行乙醇的催化氧化实验并制取乙醛(乙醛易溶于水),图中铁架台等装置已略去,粗黑线表示乳胶管.请填写下列空白:
(1)甲装置常常浸在70~80℃的水浴中,目的是
(2)由于装置设计上的缺陷,实验进行时可能会 .
(3)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接 、 接丙.

(1)B中所含官能团名称
(2)反应①类型为
(3)写出下列反应的化学方程式(注明反应条件)
①
②
③
ⅱ、一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6g,若其中水的质量为10.8g,则CO的质量为
ⅲ某课外活动小组利用如图2装置进行乙醇的催化氧化实验并制取乙醛(乙醛易溶于水),图中铁架台等装置已略去,粗黑线表示乳胶管.请填写下列空白:
(1)甲装置常常浸在70~80℃的水浴中,目的是
(2)由于装置设计上的缺陷,实验进行时可能会
(3)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接
考点:有关有机物分子式确定的计算,乙醇的化学性质
专题:实验题,烃及其衍生物的燃烧规律
分析:ⅰ、(1)根据图1分析可知 A是乙烯,B是乙醇,C是乙醛,D是乙酸,E为乙酸乙酯,据此解答;
(2)A是乙烯,F为高分子化合物,所以F为聚乙烯,发生加聚反应;
(3)①乙烯分子间发生加成聚合反应生成高分子化合物聚乙烯;
②乙醇催化氧化生成乙醛和水;
③乙酸与乙醇发生酯化反应生成乙酸乙酯和水;
ⅱ、根据反应中生成水的质量可确定乙醇的物质的量,进而求出碳原子的物质的量同时也是CO2和CO的物质的量和,再根据二者总的质量求出平均摩尔质量,最后用十字交叉法解题;
ⅲ、(1)加热时采用水浴加热可以让乙醇平稳气化成乙醇蒸气;
(2)根据反应物和生成物在水中的溶解性解答;
(3)安全瓶中的导管是“短进长出”.
(2)A是乙烯,F为高分子化合物,所以F为聚乙烯,发生加聚反应;
(3)①乙烯分子间发生加成聚合反应生成高分子化合物聚乙烯;
②乙醇催化氧化生成乙醛和水;
③乙酸与乙醇发生酯化反应生成乙酸乙酯和水;
ⅱ、根据反应中生成水的质量可确定乙醇的物质的量,进而求出碳原子的物质的量同时也是CO2和CO的物质的量和,再根据二者总的质量求出平均摩尔质量,最后用十字交叉法解题;
ⅲ、(1)加热时采用水浴加热可以让乙醇平稳气化成乙醇蒸气;
(2)根据反应物和生成物在水中的溶解性解答;
(3)安全瓶中的导管是“短进长出”.
解答:
解:ⅰ、A是气态烃,完全燃烧时产生的CO2和H2O的物质的量之比为1:1,所以A中C、H原子个数比为1:2,A的相对分子量小于30,所以A是乙烯;中间产物C含有醛基,所以C是乙醛,则B是乙醇;E有香味,说明E中含有酯基,羧酸和醇反应生成酯,所以D是乙酸;F是高分子化合物,乙烯发生加聚反应生成聚乙烯,所以F是聚乙烯,
(1)B是乙醇,分子式为:C2H5OH,所含官能团名称为羟基;E为乙酸和乙醇反应后的产物,所以E为乙酸乙酯,故答案为:羟基;乙酸乙酯;
(2)加聚反应指加成聚合反应,凡含有不饱和键(双键、叁键、共轭双键)等结构的化合物在催化剂等外加条件作用下,同种单体间相互加成形成新的共价键相连大分子的反应,A是乙烯,F为高分子化合物,所以F为聚乙烯,乙烯生成聚乙烯的反应属于加聚反应,
故答案为:加聚反应;
(3)①乙烯分子间发生加成聚合反应生成高分子化合物聚乙烯;反应的化学方程式为 ;
;
故答案为: ;
;
②乙醇催化氧化生成乙醛,反应为2C2H5OH+O2
2CH3CHO+2H2O,故答案为:2C2H5OH+O2
2CH3CHO+2H2O;
③乙酸与乙醇发生酯化反应生成乙酸乙酯和水,反应为CH3COOH+C2H5OH
CH3COOC2H5+H2O,故答案为:CH3COOH+C2H5OH
CH3COOC2H5+H2O;
ⅱ、设乙醇的物质的量为x,由C2H5OH~3H2O
1mol 54g
x 10.8g
=
,
解之得x=0.2mol,
由乙醇的分子式C2H5OH可知n(CO2)+n(CO)=0.2mol×2=0.4mol,则m(CO2)+m(CO)=27.6g-10.8g=16.8g,
=
=
=42g?mol-1
由十字交叉法可知:
 ,
,
所以m(CO)=28g?mol-1×0.4mol×
=1.4g,
故答案为:1.4;
ⅲ(1)甲装置常常浸在温度为70~80的水浴中,水浴能使容器受热均匀,能使甲中乙醇平稳气化成乙醇蒸气,故答案为:使生成乙醇蒸气的速率加快且较均匀;
(2)生成的乙醛和过量的乙醇易溶于水而使丙装置产生倒吸现象,故答案为:发生倒吸;
(3)为防止防止丁中水倒吸,安全瓶中的导气管是“短进长出”,所以乙接b,a接丙,故答案为:b;a.
(1)B是乙醇,分子式为:C2H5OH,所含官能团名称为羟基;E为乙酸和乙醇反应后的产物,所以E为乙酸乙酯,故答案为:羟基;乙酸乙酯;
(2)加聚反应指加成聚合反应,凡含有不饱和键(双键、叁键、共轭双键)等结构的化合物在催化剂等外加条件作用下,同种单体间相互加成形成新的共价键相连大分子的反应,A是乙烯,F为高分子化合物,所以F为聚乙烯,乙烯生成聚乙烯的反应属于加聚反应,
故答案为:加聚反应;
(3)①乙烯分子间发生加成聚合反应生成高分子化合物聚乙烯;反应的化学方程式为
 ;
;故答案为:
 ;
; ②乙醇催化氧化生成乙醛,反应为2C2H5OH+O2
| ||
| △ |
| ||
| △ |
③乙酸与乙醇发生酯化反应生成乙酸乙酯和水,反应为CH3COOH+C2H5OH
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
ⅱ、设乙醇的物质的量为x,由C2H5OH~3H2O
1mol 54g
x 10.8g
| 1mol |
| x |
| 54g |
| 10.8g |
解之得x=0.2mol,
由乙醇的分子式C2H5OH可知n(CO2)+n(CO)=0.2mol×2=0.4mol,则m(CO2)+m(CO)=27.6g-10.8g=16.8g,
. |
| M |
| m |
| n |
| 16.8g |
| 0.4mol |
由十字交叉法可知:
 ,
,所以m(CO)=28g?mol-1×0.4mol×
| 2 |
| 16 |
故答案为:1.4;
ⅲ(1)甲装置常常浸在温度为70~80的水浴中,水浴能使容器受热均匀,能使甲中乙醇平稳气化成乙醇蒸气,故答案为:使生成乙醇蒸气的速率加快且较均匀;
(2)生成的乙醛和过量的乙醇易溶于水而使丙装置产生倒吸现象,故答案为:发生倒吸;
(3)为防止防止丁中水倒吸,安全瓶中的导气管是“短进长出”,所以乙接b,a接丙,故答案为:b;a.
点评:本题考查了有机物的推断,正确推断A乙烯以及根据水的物质的量计算乙醇的物质的量为解答该题的关键,注意根据有机物的性质分析实验方案设计的原理,题目难度中等.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
下列物质分类都正确的一组是( )
| 碱 | 酸 | 盐 | 酸性氧化物 | |
| A | 纯碱 | 盐酸 | 烧碱 | 二氧化硫 |
| B | 烧碱 | 硫酸 | 食盐 | 一氧化碳 |
| C | 生石灰 | 醋酸 | 石灰水 | 水 |
| D | 苛性钠 | 碳酸 | 小苏打 | 三氧化硫 |
| A、A | B、B | C、C | D、D |
已知,常温下某浓度NaHSO3稀溶液的pH<7.则该稀溶液中下列粒子关系正确的是( )
| A、c(Na+)>c(HSO3-)>c(H+)>c(OH-) |
| B、c(Na+)=c(HSO3-)+2c(SO32-)+c(H2SO3) |
| C、c(OH-)+c(SO32-)=c(H2SO3)+c(H+) |
| D、c(Na+)+c(H+)=c(HSO3-)+c(OH-) |
下列各组离子中在水溶液中能大量共存的是( )
| A、Fe2+、K+、ClO-、Cl- |
| B、Ag+、Na+、Cl-、NO3- |
| C、NH4+、K+、CO32-、Br- |
| D、H+、Ca2+、CH3COO-、HCO3- |
 在100℃时,将0.40mol的二氧化氮气体充入2L抽真空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
在100℃时,将0.40mol的二氧化氮气体充入2L抽真空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据: 已知原子序数依次增大的A、B、C、D、E五种元素中有2种为非金属元素,其原子序数均小于30.其中A、B、C、E的价电子层中均有2个未成对电子,A、B同族且可以形成原子个数比为1:1的化合物BA,属于原子晶体.回答下列问题:
已知原子序数依次增大的A、B、C、D、E五种元素中有2种为非金属元素,其原子序数均小于30.其中A、B、C、E的价电子层中均有2个未成对电子,A、B同族且可以形成原子个数比为1:1的化合物BA,属于原子晶体.回答下列问题: 和
和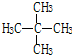
 (1)如图1所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中央滴入浓硫酸铜溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)当杠杆为绝缘体时,A端比B端
(1)如图1所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中央滴入浓硫酸铜溶液,一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑铁丝反应及两球的浮力变化)当杠杆为绝缘体时,A端比B端