题目内容
 硼化钒一空气电池是目前储电能力最高的电池,其示意图如图所示,该电池工作时的反应为4VB2+11O2═4B2O3+2V2O5.下列说法正确的是( )
硼化钒一空气电池是目前储电能力最高的电池,其示意图如图所示,该电池工作时的反应为4VB2+11O2═4B2O3+2V2O5.下列说法正确的是( )| A、电极X为电池负极 |
| B、OH-向电极X移动 |
| C、1mol VB2反应转移的电子数目是锂电池1mol Li反应转移的11倍 |
| D、VB2极的电极反应为2VB2+22e-+11H2O═2B2O3+V2O5+22OH- |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、根据原电池中负极失电子来判断;
B、原电池溶液中阴离子向负极移动;
C、根据电池总反应判断1mol VB2转移的电子,根据Li的化合价变化判断Li转移的电子数;
D、负极上是VB2失电子发生氧化反应.
B、原电池溶液中阴离子向负极移动;
C、根据电池总反应判断1mol VB2转移的电子,根据Li的化合价变化判断Li转移的电子数;
D、负极上是VB2失电子发生氧化反应.
解答:
解:A、硼化钒-空气燃料电池中,VB2在负极失电子,氧气在正极上得电子,所以X为正极,故A错误;
B、原电池中,阴离子向负极移动,阳离子向正极移动,所以溶液中的OH-向另一极移动,故B错误;
C、硼化钒一空气电池反应为4VB2+11O2═4B2O3+2V2O5,1mol VB2反应消耗
molO2转移电子数为11mol,1mol Li反应转移1mol电子,所以1mol VB2反应转移的电子数目是锂电池1mol Li反应转移的11倍,故C正确;
D、负极上是VB2失电子发生氧化反应,则VB2极发生的电极反应为:2VB2+22OH--22e-═V2O5+2B2O3+11H2O,故D错误.
故选C.
B、原电池中,阴离子向负极移动,阳离子向正极移动,所以溶液中的OH-向另一极移动,故B错误;
C、硼化钒一空气电池反应为4VB2+11O2═4B2O3+2V2O5,1mol VB2反应消耗
| 11 |
| 4 |
D、负极上是VB2失电子发生氧化反应,则VB2极发生的电极反应为:2VB2+22OH--22e-═V2O5+2B2O3+11H2O,故D错误.
故选C.
点评:本题考查原电池的工作原理,题目难度中等,本题注意把握电极反应式的书写和电子守恒的应用,正确判断离子的定向移动.

练习册系列答案
相关题目
自瑞士ETH天文研究所的Ansgar Grimberg等的研究结果表明,太阳气体中存在大量的20Ne和22Ne.下列关于20Ne和22Ne的说法正确的是( )
| A、20Ne和22Ne互为同位素 |
| B、20Ne和22Ne是同一种核素 |
| C、20Ne的原子核中有20个质子 |
| D、22Ne的原子核中有22个中子 |
化学无处不在,下列与化学有关的说法不正确的是( )
| A、“日照香炉生紫烟”的“烟”是瀑布的细小水珠形成的水雾,属于胶体 |
| B、“大漠孤烟直”的“烟”是燃烧柳枝时产生的烟,这类染料在燃烧过程中会产生污染空气的烟雾 |
| C、“月朦胧,鸟朦胧,空气雾霾浓.山朦胧,树朦胧,喉咙有点痛”,二氧化硫、氮氧化合物以及可吸入颗粒物是雾霾的主要组成,而前两项主要来自于汽车尾气的排放 |
| D、“塞翁失马焉知非福”说的是用辩证的观点看待事物,一分为二,比如SO2虽然是空气污染气体之一,但也可以被用于消毒杀菌 |
如图所示,甲池的总反应式为:N2H4+O2═N2+2H2O下列关于该电池工作时说法正确的是( )


| A、甲池中负极反应为:N2H4-4e-═N2+4H+ |
| B、甲池溶液pH不变,乙池溶液pH减小 |
| C、甲池中消耗2.24L O2,此时乙池中理论上最多产生12.8g固体 |
| D、反应一段时间后,向乙池中加一定量CuO固体,能使CuSO4溶液恢复到原浓度 |
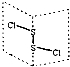 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体.下列说法错误的是( )
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体.下列说法错误的是( )| A、S2Cl2的结构中各原子均达到8电子的稳定结构 |
| B、S2Cl2为含有极性键和非极性键的共价化合物 |
| C、若S2Br2与S2Cl2结构相似,则熔沸点:S2Cl2>S2Br2 |
| D、S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl |
可以用分液漏斗分离的一组混合物是( )
| A、酒精和碘 | B、溴和四氯化碳 |
| C、乙酸和水 | D、苯和水 |
生活处处有化学.下列说法正确的是( )
| A、利用60Co的放射性可治疗某些疾病.60Co和59Co互为同位素 |
| B、明矾净水和“84”消毒液消毒的原理相同 |
| C、碳酸钡、硫酸钡等难溶性钡盐均可用于钡餐透视 |
| D、月饼包装盒中常放入铁粉作干燥剂 |