题目内容
下列变化可通过一步化学反应实现的是( )
| A、N2→NO2 |
| B、Al2O3→Al(OH)3 |
| C、S→SO3 |
| D、SiO2→SiF4 |
考点:氮气的化学性质,硅和二氧化硅,两性氧化物和两性氢氧化物
专题:
分析:A.氮气和氧气在放电条件下反应生成NO,NO和氧气反应生成NO2;
B.氧化铝和水不反应;
C.S在空气中燃烧生成二氧化硫,二氧化硫和氧气在催化剂、加热条件下反应生成SO3;
D.二氧化硅和HF反应生成SiO2→SiF4.
B.氧化铝和水不反应;
C.S在空气中燃烧生成二氧化硫,二氧化硫和氧气在催化剂、加热条件下反应生成SO3;
D.二氧化硅和HF反应生成SiO2→SiF4.
解答:
解:A.氮气和氧气在放电条件下反应生成NO,NO和氧气反应生成NO2,所以不能一步发生反应N2→NO2,故A错误;
B.氧化铝和水不反应,所以不能一步发生反应Al2O3→Al(OH)3,故B错误;
C.S在空气中燃烧生成二氧化硫,二氧化硫和氧气在催化剂、加热条件下反应生成SO3,所以不能一步发生反应S→SO3,故C错误;
D.二氧化硅和HF反应生成SiO2→SiF4,所以能一步发生反应SiO2→SiF4,故D正确.
故选D.
B.氧化铝和水不反应,所以不能一步发生反应Al2O3→Al(OH)3,故B错误;
C.S在空气中燃烧生成二氧化硫,二氧化硫和氧气在催化剂、加热条件下反应生成SO3,所以不能一步发生反应S→SO3,故C错误;
D.二氧化硅和HF反应生成SiO2→SiF4,所以能一步发生反应SiO2→SiF4,故D正确.
故选D.
点评:本题考查物质之间转化,明确物质性质是解本题关键,知道物质转化时的反应条件,注意二氧化硅性质的特殊性,题目难度不大.

练习册系列答案
相关题目
在容积固定的密闭容器中存在如下反应:A(g)+3B(g)?2C(g)△H<0.某研究小组研究其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断正确的是( )
A、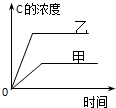 研究的是温度对反应的影响,且乙的温度较高 |
B、 研究的是压强对反应的影响,且甲的压强较高 |
C、 研究的是温度对反应的影响,且乙的温度较低 |
D、 研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高 |
下列离子方程式书写正确的是( )
| A、铝片放入NaOH溶液中:2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑ |
| B、NaHCO3电离:NaHCO3?Na++H++CO32- |
| C、醋酸与碳酸钠反应:2H++CO32-=CO2↑+H2O |
| D、铜与氯化铁溶液反应:Fe3++Cu=Cu2++Fe2+. |
 把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )
把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )| A、X为CO2,Y为Ca(OH)2 |
| B、X为NH3?H2O,Y为AlCl3 |
| C、X为NaOH,Y为AlCl3 |
| D、X为HCl,Y为NaAlO3 |
室温下,某溶液中由水电离出来的c(OH-)=10-12mol?L-1,则该溶液的溶质不可能是( )
| A、HCl |
| B、NaOH |
| C、NH4NO3 |
| D、H2SO4 |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、将0.1 molFeCL3溶液于1 L水中,所得溶液含Fe3+离子数目为0.1 NA |
| B、1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA |
| C、常温、常压下,4.6 g NO2和N2O4混合气体中含有的氧原子数目为0.2NA |
| D、在高温下,有1 mol Fe与足量的水蒸气反应,转移电子的数目为3NA |
 金属及其化合物在人类生活、生产中发挥着重要的作用.
金属及其化合物在人类生活、生产中发挥着重要的作用.