题目内容
芳樟醇是贵重的香料,它可由多种方法合成.
(1)芳樟醇的一种工业合成路线如下:
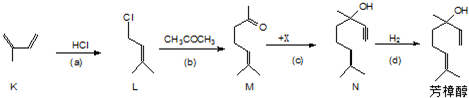
①上图中K的名称是: ;反应(b)的类型是: .
②已知c是加成反应,反应c中另一反应物X的结构式为: .
③L的同分异构体很多,其中只含一个甲基的链状同分异构体有: 种(不考虑立体异构).
(2)芳樟醇的另一种常见合成路线如下:β一菠烯在600~700℃时可以开环生成月桂烯,月桂烯与HCl加成后再与CH3COONa反应转化为芳樟醇的乙酸酯,最后经水解得到芳樟醇.

1A的结构简式为: ;②反应(c)的化学方程式为: .
(1)芳樟醇的一种工业合成路线如下:

①上图中K的名称是:
②已知c是加成反应,反应c中另一反应物X的结构式为:
③L的同分异构体很多,其中只含一个甲基的链状同分异构体有:
(2)芳樟醇的另一种常见合成路线如下:β一菠烯在600~700℃时可以开环生成月桂烯,月桂烯与HCl加成后再与CH3COONa反应转化为芳樟醇的乙酸酯,最后经水解得到芳樟醇.

1A的结构简式为:
考点:有机物的合成
专题:有机物的化学性质及推断
分析:(1)①根据K的结构简式进行命名,比较L和M的结构可判断反应类型;
②比较M和N的结构,利用元素守恒判断;
③根据条件及碳链异和官能团位置异构可判断;
(2)月桂烯与HCl加成后再与CH3COONa反应转化为芳樟醇的乙酸酯,比较芳樟醇的结构和月桂烯的结构可知,月桂烯与一分子HCl发生加成反应,且氯原子加在芳樟醇中羟基的位置,据此可推知A的结构为 ,
, 与CH3COONa反应得B为
与CH3COONa反应得B为 ,
, 在碱性条件下发生酯的水解得芳樟醇,据此答题;
在碱性条件下发生酯的水解得芳樟醇,据此答题;
②比较M和N的结构,利用元素守恒判断;
③根据条件及碳链异和官能团位置异构可判断;
(2)月桂烯与HCl加成后再与CH3COONa反应转化为芳樟醇的乙酸酯,比较芳樟醇的结构和月桂烯的结构可知,月桂烯与一分子HCl发生加成反应,且氯原子加在芳樟醇中羟基的位置,据此可推知A的结构为
 ,
, 与CH3COONa反应得B为
与CH3COONa反应得B为 ,
, 在碱性条件下发生酯的水解得芳樟醇,据此答题;
在碱性条件下发生酯的水解得芳樟醇,据此答题;解答:
解:(1)①根据K的结构简式可知,K的命称为2-甲基-1,3-丁二烯(或:异戊二烯),比较L和M的结构可知反应(b)是取代反应,
故答案为:2-甲基-1,3-丁二烯(或:异戊二烯);取代反应;
②比较M和N的结构,利用元素守恒可知X为CH≡CH,
故答案为:CH≡CH;
③根据L的结构可知,L中有一个碳碳双键和一个氯原子,所以只含一个甲基的链状同分异构体可以是碳链为C-C-C-C-C,然后将-Cl和碳碳双键的位置在上面移动可得6种结构,也可以是碳链为C-C-C(-C)-C,然后将-Cl和碳碳双键的位置在上面移动可得3种结构,所以共有9种,
故答案为:9;
(2)月桂烯与HCl加成后再与CH3COONa反应转化为芳樟醇的乙酸酯,比较芳樟醇的结构和月桂烯的结构可知,月桂烯与一分子HCl发生加成反应,且氯原子加在芳樟醇中羟基的位置,据此可推知A的结构为 ,
, 与CH3COONa反应得B为
与CH3COONa反应得B为 ,
, 在碱性条件下发生酯的水解得芳樟醇,
在碱性条件下发生酯的水解得芳樟醇,
①根据上面的分析可知,A为 ,②反应(c)的化学方程式为
,②反应(c)的化学方程式为 ,
,
故答案为:① ; ②
; ② ;
;
故答案为:2-甲基-1,3-丁二烯(或:异戊二烯);取代反应;
②比较M和N的结构,利用元素守恒可知X为CH≡CH,
故答案为:CH≡CH;
③根据L的结构可知,L中有一个碳碳双键和一个氯原子,所以只含一个甲基的链状同分异构体可以是碳链为C-C-C-C-C,然后将-Cl和碳碳双键的位置在上面移动可得6种结构,也可以是碳链为C-C-C(-C)-C,然后将-Cl和碳碳双键的位置在上面移动可得3种结构,所以共有9种,
故答案为:9;
(2)月桂烯与HCl加成后再与CH3COONa反应转化为芳樟醇的乙酸酯,比较芳樟醇的结构和月桂烯的结构可知,月桂烯与一分子HCl发生加成反应,且氯原子加在芳樟醇中羟基的位置,据此可推知A的结构为
 ,
, 与CH3COONa反应得B为
与CH3COONa反应得B为 ,
, 在碱性条件下发生酯的水解得芳樟醇,
在碱性条件下发生酯的水解得芳樟醇,①根据上面的分析可知,A为
 ,②反应(c)的化学方程式为
,②反应(c)的化学方程式为 ,
,故答案为:①
 ; ②
; ② ;
;
点评:本题考查有机物的推断与合成,难度中等,答题时注意反应中官能团的变化,根据芳樟醇的结构,采取逆推法确定A的结构,(1)中③同分异构体的判断为本题难点.

练习册系列答案
相关题目
下列属于物理变化的是( )
| A、氯气溶于水 | B、食物变质 |
| C、焰色反应 | D、光合作用 |
对于药品的使用和作用,下列说法正确的是( )
| A、用药要慎重,不得使用变质或过期的药品 |
| B、毒品就是有毒的药品 |
| C、我国明代医学家李时珍所著的医学名著是《神农本草经》 |
| D、海洛英不是国际奥委会严格禁止使用的兴奋剂 |
下列混和物的分离,可用溶解-过滤-蒸发操作的是( )
| A、混有泥沙的粗盐 |
| B、水和酒精 |
| C、四氯化碳和水 |
| D、铁粉和铝粉 |
下列叙述正确的是( )
| A、电解NaCl溶液时,阴极产生1mol Cl2的同时阳极产生1mol H2 |
| B、0.1mol?L-1 AlCl3溶液中Al3+的浓度为0.1mol?L-1 |
| C、7g 14C中所含中子数为4NA(设NA为阿伏加德罗常数的值) |
| D、2.24L氯气与足量NaOH稀溶液反应,转移0.1mol电子 |
下列说法中正确的是( )
| A、煤燃烧是化学能转化为光能的过程 |
| B、1 mol 甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
| C、HCl 和 NaOH 反应的中和热△H=-57.3 kJ/mol,则H2SO4和 Ca(OH)2 反应的中和热△H=2×(-57.3)kJ?mol-1 |
| D、反应 H2(g)+F2(g)═2HF(g);△H=-270 kJ?mol-1说明在相同条件下,1 mol 氢气与 1 mol 氟气的能量总和大于2 mol 氟化氢气体的能量 |
既能与盐酸反应,又能与氢氧化钠溶液反应的化合物是( )
①Al(OH)3 ②Al2O3 ③Al ④NaHCO3 ⑤Mg(OH)2.
①Al(OH)3 ②Al2O3 ③Al ④NaHCO3 ⑤Mg(OH)2.
| A、①③④⑤ | B、①②③④⑤ |
| C、①②③④ | D、①②④⑤ |


 中官能团的名称
中官能团的名称 含苯环的同分异构体的结构简式
含苯环的同分异构体的结构简式
 分子中含有氯原子,按实验操作顺序,依次需要加入的试剂是
分子中含有氯原子,按实验操作顺序,依次需要加入的试剂是