题目内容
已知:H2O?H++OH-(△H>0),KW为水的电离常数,完成下表.
| 改变条件 | 电离平衡移动方向 | 溶液中c(H+) | PH的变化 | KW |
| 升高温度 | ||||
| 加入酸 | ||||
| 加入Na |
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:水的电离是吸热过程,升温,平衡正向进行,酸碱抑制水的电离平衡,水解的盐促进水的电离,离子积常数随温度变化,溶液PH是利用氢离子浓度的负对数计算分析判断.
解答:
解:H2O?H++OH-(△H>0),KW为水的电离常数,水的电离是吸热过程,升温,平衡正向进行,酸碱抑制水的电离平衡,水解的盐促进水的电离,离子积常数随温度变化;
升温平衡正向进行,氢离子浓度增大,溶液PH减小,Kw增大;
加入酸,平衡逆向进行,氢离子浓度增大,PH减小,Kw不变;
加入Na,和水中氢离子反应生成氢气,平衡正向进行,氢离子浓度减小,溶液PH增大,Kw不变;
故答案为:
升温平衡正向进行,氢离子浓度增大,溶液PH减小,Kw增大;
加入酸,平衡逆向进行,氢离子浓度增大,PH减小,Kw不变;
加入Na,和水中氢离子反应生成氢气,平衡正向进行,氢离子浓度减小,溶液PH增大,Kw不变;
故答案为:
| 升高温度 | 正向 | 增大 | 减小 | 增大 |
| 加入酸 | 逆向 | 增大 | 减小 | 不变 |
| 加入Na | 正向 | 减小 | 增大 | 不变 |
点评:本题考查了水的电离影响因素分析判断,掌握基础是关键,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各组物质中,相互间一定互为同分异构体的是( )
| A、淀粉和纤维素 |
| B、蔗糖和麦芽糖 |
| C、C4H6和C5H8 |
| D、氨基酸和蛋白质 |
对于可逆反应2A+3B?2C;△H<0,下列条件的改变一定可以加快正反应速率的是( )
| A、增加压强 |
| B、升高温度 |
| C、增加A的量 |
| D、加入二氧化锰作催化剂 |

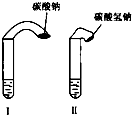 (1)高中教材中有这样一个实验:在两支试管中分别加入3mL稀盐酸(均足量)(只有浓度小于1mol?L-1的稀盐酸跟Na2CO3和NaHCO3反应才能根据反应的剧烈程度区分开来,浓度较高则反应现象都是同样的剧烈),将两个各装有0.3g NaHCO3和Na2CO3粉末的小气球分别套在两支试管口上.将气球内的NaHCO3和Na2CO3同时倒入试管中,观察到现象如下:
(1)高中教材中有这样一个实验:在两支试管中分别加入3mL稀盐酸(均足量)(只有浓度小于1mol?L-1的稀盐酸跟Na2CO3和NaHCO3反应才能根据反应的剧烈程度区分开来,浓度较高则反应现象都是同样的剧烈),将两个各装有0.3g NaHCO3和Na2CO3粉末的小气球分别套在两支试管口上.将气球内的NaHCO3和Na2CO3同时倒入试管中,观察到现象如下:
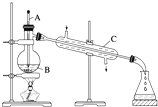 选择下列实验方法分离物质,将分离方法的序号填在横线上.
选择下列实验方法分离物质,将分离方法的序号填在横线上.