题目内容
11.在一定条件下,对于在密闭容器中进行的反应P(g)+Q(g)?R(g)+S(g),下列说法中可以充分说明这一反应已经达到平衡状态的是( )| A. | P、Q、R、S的浓度相等 | B. | P、Q、R、S在容器中共存 | ||
| C. | P、Q的反应速率相等内部 | D. | P、Q、R、S的浓度不再变化 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、当体系达平衡状态时,P、Q、R、S的浓度可能相等,也可能不等,与各物质的初始浓度及转化率有关,故A错误;
B、只要反应发生就是反应物和生成物共存的体系,故B错误;
C、只要反应发生P、Q的反应速率一直相等,故C错误;
D、P、Q、R、S的浓度不再变化,说明各物质的量不变,反应达平衡状态,故D正确;
故选D.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
1.某研究性学习小组为了探究醋酸的电离情况,进行了如下实验.
实验一 配制并标定醋酸溶液的浓度
取冰醋酸配制250mL 0.2mol/L的醋酸溶液,用0.2mol/L的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定.回答下列问题:
(1)配制250mL 0.2mol/L 醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和250mL容量瓶.
(2)为标定某醋酸溶液的准确浓度,用0.2000mol/L的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
则该醋酸溶液的准确浓度为0.2000mol/L.
实验二 探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
回答下列问题:
(3)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是0.010 0 mol•L-1醋酸的pH大于2或醋酸稀释10倍时,pH的变化值小于1
(4)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度增大.
实验三 探究温度对醋酸电离程度的影响
(5)请你设计一个实验完成该探究,请简述你的实验方案用pH计(或精密pH试纸)测定相同浓度的醋酸在几种不同温度时的pH.
实验一 配制并标定醋酸溶液的浓度
取冰醋酸配制250mL 0.2mol/L的醋酸溶液,用0.2mol/L的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定.回答下列问题:
(1)配制250mL 0.2mol/L 醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和250mL容量瓶.
(2)为标定某醋酸溶液的准确浓度,用0.2000mol/L的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.02 | 20.00 | 18.80 | 19.98 |
实验二 探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
| 醋酸浓度(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
(3)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是0.010 0 mol•L-1醋酸的pH大于2或醋酸稀释10倍时,pH的变化值小于1
(4)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度增大.
实验三 探究温度对醋酸电离程度的影响
(5)请你设计一个实验完成该探究,请简述你的实验方案用pH计(或精密pH试纸)测定相同浓度的醋酸在几种不同温度时的pH.
2.分子式为C7H12O4的酯,在酸性条件下水解生成一种二元有机酸X和一种醇Y,下列有关有机酸X和醇Y的结构数目正确的是( )
| 选项 | 有机酸X的数目 | 醇Y的数目 |
| A | 4种 | 3种 |
| B | 4种 | 2种 |
| C | 5种 | 3种 |
| D | 5种 | 2种 |
| A. | A | B. | B | C. | C | D. | D |
19.下列操作成装置能达到实验目的是( )
| A. | 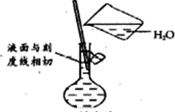 制溶液 | B. | 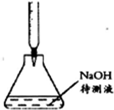 中和滴定 | ||
| C. | 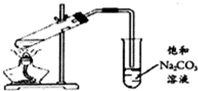 制备乙醇乙酯 | D. | 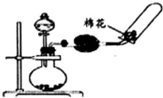 制备收集干燥的氨气 |
6.下列说法中正确的是( )
| A. | 铝的第一电离能比镁的第一电离能大 | |
| B. | 钾的第一电离能比镁的第一电离能大 | |
| C. | 在所有的元素中,F的第一电离能最大 | |
| D. | 第3周期所含元素中钠的第一电离能最小 |
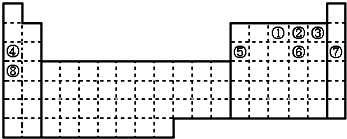
16.下列各组元素中,按最高正化合价递增顺序排列的是( )
①C、N、F ②Na、Mg、Al ③F、Cl、Br ④P、S、Cl.
①C、N、F ②Na、Mg、Al ③F、Cl、Br ④P、S、Cl.
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
20.下列有关说法正确的是( )
| A. | 乙酸乙酯在碱性条件下的水解反应称为皂化反应 | |
| B. | 乙烷、苯、葡萄糖溶液均不能使酸性高锰酸钾溶液褪色 | |
| C. | 苯的密度比水小,但由苯反应制得的溴苯、硝基苯、环己烷的密度都比水大 | |
| D. | 2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物种类相同 |
 ;(2)NaOH
;(2)NaOH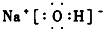 ;(3)HClO
;(3)HClO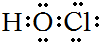 ;(4)H2O2
;(4)H2O2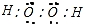 .
.