题目内容
下列判断正确的是
A.酸酐一定是氧化物 B.晶体中一定存在化学键
C.碱性氧化物一定是金属氧化物 D.正四面体分子中键角一定是109o28′
C
【解析】
试题分析:A、酸酐不一定是氧化物,如乙酸的酸酐是2分子乙酸 脱去1分子水得到的物质,不属于氧化物,错误;B、稀有气体对应的晶体中不含任何化学键,错误;C、碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物,正确;D、白磷分子的空间构型是正四面体,但键角是60 o,错误,答案选C。
考点:考查对酸酐、氧化物、晶体中的化学键、键角的判断

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
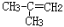 C.CH3CH2CH2COOH D.
C.CH3CH2CH2COOH D.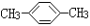
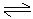 KI3
KI3