题目内容
把500ml含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀:另取一份加入含b mol硝酸银的溶液,恰好使卤离子完全沉淀,则该混合溶液中钾离子浓度为
A.0.1(b-2a)mol·L-1 B.10(2a-b) mol·L-1
C.10(b-a) mol·L-1 D.10(b-2a) mol·L-1
D
【解析】
试题分析:500mL溶液分成5等分,每份是100mL,第一份溶液说明钡离子的物质的量是amol,第二份溶液说明氯离子的物质的量是bmol,根据电荷守恒可知一份溶液中钾离子的物质的量是(b-2a)mol,所以原混合液中钾离子的物质的量浓度是(b-2a)mol/0.1L=10(b-2a)mol/L,答案选D。
考点:考查溶液中离子浓度的计算

练习册系列答案
相关题目

 中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1mol/L乙溶液中c(H+)>0.1mol/L;③向丙溶液中滴入
中的不同阳离子和阴离子各一种组成。已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1mol/L乙溶液中c(H+)>0.1mol/L;③向丙溶液中滴入 溶液有不溶于稀
溶液有不溶于稀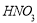 的白色沉淀生成,下列结论不正确的是
的白色沉淀生成,下列结论不正确的是  B.乙溶液含有
B.乙溶液含有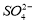 C.丙溶液含有
C.丙溶液含有 D.丁溶液含有
D.丁溶液含有