��Ŀ����
����ѧ����ѡ��2����ѧ�뼼������15�֣�
�л��ϳ��г��õ��٣�����̿����������ʹ�ã��ᱻ�����л��������������Ⱦ��ʧȥ���ԣ���Ϊ�ϴ�����һ���ɷϴ�����ȡPdCl2�Ĺ����������£�
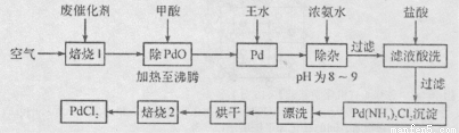
��1��������1��ͨ�������Ŀ����ʹ�л����������̿�ȿ�ȼ��ͨ��ȼ�ն�������ͨ��������෴��������ʵ��Ŀ�ģ���ԭ���� ��
��2�������ڷ�Ӧ�б�����Ϊ������̼��д��������PdO��Ӧ�Ļ�ѧ����ʽ��___ ��
��3����Ũ��ˮʱ����ת��Ϊ������[Pd��NH3��4]2+����ʱ���Ĵ�����ʽ�� ��д��ѧʽ����
��4������Ũ��ˮ�Ĺ����У���Ҫ������Һ��pHΪ8��9��ʵ���Ҽ����ҺpH�IJ��������ǣ� ��
��5��������2����Ŀ���ǣ� ��
��6���뱺��2�������������Ԫ����ͬ�Ļ������� ��������������γ�һ�ֻ����ͼ���ȼ�ϵ�أ��为����ӦʽΪ______________________________��
��7�� Pd�м�����ˮ�ķ�Ӧ���Ա�ʾΪPd+HCl+HNO3��A+B��+H2O��δ��ƽ��������BΪ��ɫ�ж����壬�������ڿ����в����ȶ����ڣ�A�к�������Ԫ�أ�����PdԪ�ص���������Ϊ42.4%��HԪ�ص���������Ϊ0.8%����A�Ļ�ѧʽΪ ��
��1�������Ŀ�������ߴ������ȣ�ʹ��Ӧ�����¶ȹ��ͣ��������ܷ�����Ӧ����2�֣�
��2�� HCOOH��PdO Pd��CO2����H2O��2�֣�
Pd��CO2����H2O��2�֣�
��3��Fe(OH)3��2�֣�
��4���ýྻ�IJ�����պȡ����Һ����pH��ֽ�ϣ������ɫ����ɫ������pH��2�֣�
��5���Ѱ���ʹ Pd(NH3)2Cl2����PdCl2����2�֣�
��6��N2H4����1�֣�N2H4+4OH�D�D4e��==N2��+4H2O��2�֣�
��7�� H2PdCl4��2�֣�
��������
�����������1��������1��ͨ�������Ŀ����ʹ�л����������̿�ȿ�ȼ��ͨ��ȼ�ն���������ͨ�������������Ŀ�������ߴ������ȣ�ʹ��Ӧ�����¶ȹ��ͣ��������ܷ�����Ӧ����˷���������ʵ��Ŀ�ģ���2�������ڷ�Ӧ�б�����Ϊ������̼���������PdO��Ӧ�Ļ�ѧ����ʽ��HCOOH��PdO Pd��CO2����H2O����3������Ũ��ˮʱ����Һ�е�Fe3+�ͻᷢ��������Ӧ����Fe(OH)3�������䷴Ӧ�����ַ���ʽ�ǣ�Fe3++3 NH3��H2O= Fe(OH)3��+3NH4+����4������Ũ��ˮ�Ĺ����У���Ҫ������Һ��pHΪ8��9��ʵ���Ҽ����ҺpH�IJ����������ýྻ�IJ�����պȡ����Һ����pH��ֽ�ϣ������ɫ����ɫ������pH����5��������2����Ŀ����ʹ Pd(NH3)2Cl2����PdCl2���������Ѱ���������6���뱺��2����������NH3���Ԫ����ͬ�Ļ�������N2H4��������������γ�һ�ֻ����ͼ���ȼ�ϵ�أ��为����N2H4ʧȥ���ӱ���������ӦʽΪN2H4+4OH�D�D4e��==N2��+4H2O����7�� Pd�м�����ˮ�ķ�Ӧ���Ա�ʾΪPd+HCl+HNO3��A+B��+H2O��δ��ƽ��������BΪ��ɫ�ж����壬�������ڿ����в����ȶ����ڣ���B��NO��A�к�������Ԫ�أ�����PdԪ�ص���������Ϊ42.4%��HԪ�ص���������Ϊ0.8%������ǰ�ߵ�֪ʶ��֪�ڷ�Ӧ��Pd��Ӧ���Ϊ+2�ۣ�����������ԭ��Ӧ�л��ϼ�����������ȿ�֪������ʽ��Pd�������ϵ���ֱ���3��2������Ԫ�ص�ԭ���غ㣬��ϻ��������������ϼ۵Ĵ�����Ϊ0��֪��A�к��е�Ԫ����Pd��H��Cl��������������100,���ǵĸ�����Ϊ��n(Pd)��n(H):n(Cl)=(42.4��106): (0.8��1):[(100-42.4��0.8)��35.5] = 0.4:0.8: 1.6=1��2��4������A�Ļ�ѧʽΪH2PdCl4��
Pd��CO2����H2O����3������Ũ��ˮʱ����Һ�е�Fe3+�ͻᷢ��������Ӧ����Fe(OH)3�������䷴Ӧ�����ַ���ʽ�ǣ�Fe3++3 NH3��H2O= Fe(OH)3��+3NH4+����4������Ũ��ˮ�Ĺ����У���Ҫ������Һ��pHΪ8��9��ʵ���Ҽ����ҺpH�IJ����������ýྻ�IJ�����պȡ����Һ����pH��ֽ�ϣ������ɫ����ɫ������pH����5��������2����Ŀ����ʹ Pd(NH3)2Cl2����PdCl2���������Ѱ���������6���뱺��2����������NH3���Ԫ����ͬ�Ļ�������N2H4��������������γ�һ�ֻ����ͼ���ȼ�ϵ�أ��为����N2H4ʧȥ���ӱ���������ӦʽΪN2H4+4OH�D�D4e��==N2��+4H2O����7�� Pd�м�����ˮ�ķ�Ӧ���Ա�ʾΪPd+HCl+HNO3��A+B��+H2O��δ��ƽ��������BΪ��ɫ�ж����壬�������ڿ����в����ȶ����ڣ���B��NO��A�к�������Ԫ�أ�����PdԪ�ص���������Ϊ42.4%��HԪ�ص���������Ϊ0.8%������ǰ�ߵ�֪ʶ��֪�ڷ�Ӧ��Pd��Ӧ���Ϊ+2�ۣ�����������ԭ��Ӧ�л��ϼ�����������ȿ�֪������ʽ��Pd�������ϵ���ֱ���3��2������Ԫ�ص�ԭ���غ㣬��ϻ��������������ϼ۵Ĵ�����Ϊ0��֪��A�к��е�Ԫ����Pd��H��Cl��������������100,���ǵĸ�����Ϊ��n(Pd)��n(H):n(Cl)=(42.4��106): (0.8��1):[(100-42.4��0.8)��35.5] = 0.4:0.8: 1.6=1��2��4������A�Ļ�ѧʽΪH2PdCl4��
���㣺����ʵ�������Ŀ�ġ���������ҺpH�ļ��鷽������ѧ����ʽ�����ӷ���ʽ����д��ȼ�ϵ�صĸ���ԭ�������ʻ�ѧʽ��ȷ����֪ʶ��

 ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д����и���ʵ��������������ó��Ľ�����ȷ����
| ʵ����� | ʵ������ | ���� |
A | ������ϡH2SO4���ȣ��ټ��� ����Һˮԡ���� | ���������� | ����ˮ�������ԭ�� |
B | ��ij��Һ���ȵμ���ˮ���ٵ� ������KSCN��Һ | ��Һ���Ѫ��ɫ | ��Һ�к���Fe2+ |
C | ��NaAlO2��Һ�еμӱ��� NaHCO3��Һ |
�а�ɫ�������� | ��֤���߶�������ˮ�ⷴ Ӧ������ٽ� |
D | ��CO2ͨ��Na2SiO3��Һ�� | �а�ɫ�������� | ֤��H2CO3���Ա�H2SiO3ǿ |
 2KCl��3O2��
2KCl��3O2�� K2MnO4��MnO2��O2��
K2MnO4��MnO2��O2�� 2H2����O2��
2H2����O2��
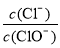 ��ֵ���¶ȸߵ��йء���n(KOH)��a molʱ�������й�˵���������(����)
��ֵ���¶ȸߵ��йء���n(KOH)��a molʱ�������й�˵���������(����)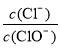 ��11������Һ��
��11������Һ��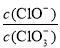 ��
��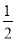
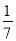 mol
mol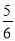 a mol
a mol