题目内容
14.已知反应:16HCl(浓)+2KMnO4═2MnCl2+8H2O+2KCl+5Cl2↑该反应中的氧化剂是KMnO4(填写化学式).氧化产物与还原产物的物质的量之比为5:2;若产生的气体在标准状况下体积为2.24L,则反应过程中转移电子的数目为0.2 NA,被氧化的盐酸的物质的量是0.2mol.用单线桥描述该反应的电子转移:16HCl(浓)+2KMnO4═2MnCl2+8H2O+2KCl+5Cl2↑
分析 2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O中,Mn元素的化合价降低,Cl元素的化合价升高,则HCl为还原剂,对应氧化产物为Cl2,据此计算氧化产物与还原产物的物质的量之比,根据化合价的升降确定电子转移的情况.
解答 解:2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O中,Mn元素的化合价降低,氧化剂为KMnO4,对应还原产物为MnCl2,Cl元素的化合价升高,则HCl为还原剂,对应氧化产物为Cl2,氧化产物与还原产物的物质的量之比为5:2,若产生的气体1mol,则反应过程中转移电子10mol,若产生的气体在标准状况下体积为2.24L即0.1mol,则反应过程中转移电子为0.2 NA,被氧化的盐酸和参加反应的盐酸物质的量之比是10:16=5:8,若产生的气体在标准状况下体积为2.24L即0.1mol,消耗盐酸是0.32mol,被氧化的盐酸的物质的量是0.2mol,电子转移如下: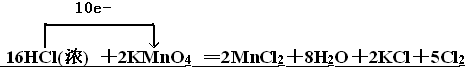 .
.
故答案为:KMnO4;5:2;0.2;0.2mol;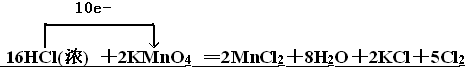 .
.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应中基本概念,题目难度不大.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
4. 25℃时,在20ml 0.1mol•L-1NaOH溶液中逐滴加入0.2mol•L-1醋酸溶液,滴定曲线如图所示,有关粒子浓度的关系中,不正确的是( )
25℃时,在20ml 0.1mol•L-1NaOH溶液中逐滴加入0.2mol•L-1醋酸溶液,滴定曲线如图所示,有关粒子浓度的关系中,不正确的是( )
 25℃时,在20ml 0.1mol•L-1NaOH溶液中逐滴加入0.2mol•L-1醋酸溶液,滴定曲线如图所示,有关粒子浓度的关系中,不正确的是( )
25℃时,在20ml 0.1mol•L-1NaOH溶液中逐滴加入0.2mol•L-1醋酸溶液,滴定曲线如图所示,有关粒子浓度的关系中,不正确的是( )| A. | 在A点:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | B. | 在B点:c(Na+)﹦c(CH3COO-)>c(OH-)﹦c(H+) | ||
| C. | 在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | D. | 在C点:c(CH3COO-)+c(CH3COOH)﹦2 c(Na+) |
9.以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如表.
表1 几种砷酸盐的Ksp
表2 工厂污染物排放浓度及允许排放标准
回答以下问题:
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=0.29mol/L.
(2)向Al3+、Fe3+的混合溶液中加入Na3AsO4溶液,当两种沉淀共存时,溶液中c(Al3+)和c(Fe3+)的比值为2.8×104.
(3)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降.
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为CaSO4.
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为H3AsO4是弱酸,当溶液中pH调节到8左右时,酸碱反应,使溶液中AsO43-浓度增大,至Qc>Ksp,Ca3(AsO4)2开始沉淀.
表1 几种砷酸盐的Ksp
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| AlAsO4 | 1.6×10-16 |
| FeAsO4 | 5.7×10-21 |
| 污染物 | H2SO4 | As |
| 浓度 | 28.42g•L-1 | 1.6g/L |
| 排放标准 | pH=6~9 | 0.5mg/L |
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=0.29mol/L.
(2)向Al3+、Fe3+的混合溶液中加入Na3AsO4溶液,当两种沉淀共存时,溶液中c(Al3+)和c(Fe3+)的比值为2.8×104.
(3)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降.
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为CaSO4.
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为H3AsO4是弱酸,当溶液中pH调节到8左右时,酸碱反应,使溶液中AsO43-浓度增大,至Qc>Ksp,Ca3(AsO4)2开始沉淀.