题目内容
5.化学实验装置的科学设计是实验是否取得预期效果的关键.请回答下列有关实验装置的相关问题.如图A为“人教版”教材制备乙酸乙酯的实验装置,某同学甲认为图B装置进行酯化反应效果比A要好,他的理由是便于冷凝回流,减少反应物损失;某同学乙经查阅资料认为图C装置进行酯化反应效果更好,他的理由是既能冷凝回流又能及时分离出反应生成的水,有利于酯的生成.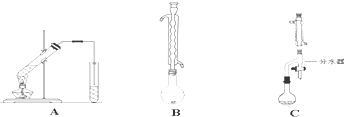
分析 图B装置中冷凝管可使有机物冷凝回流,提高利用率;图C装置除冷凝回流,且能分离出水,利用酯化反应正向移动,以此来解答.
解答 解:同学甲认为图B装置进行酯化反应效果比A要好,他的理由是便于冷凝回流,减少反应物损失;
同学乙经查阅资料认为图C装置进行酯化反应效果更好,他的理由是既能冷凝回流又能及时分离出反应生成的水,有利于酯的生成,
故答案为:便于冷凝回流,减少反应物损失;既能冷凝回流又能及时分离出反应生成的水,有利于酯的生成.
点评 本题考查实验装置的综合应用及乙酸乙酯制备,为高频考点,把握图中装置的作用、实验原理为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
15.下列指定反应的离子方程式正确的是( )
| A. | 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O=H2SiO3↓+SO32- | |
| B. | 向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 向Al2(SO4)3溶液中加入过量的NH3•H2O:Al3++4NH3•H2O=[Al(OH)4]-+4NH4+ | |
| D. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑ |
16.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 23gNa由原子变成离子时,失去电子数为0.2NA | |
| B. | 18gH2O所含电子数为10NA | |
| C. | 1mol氯气与足量的NaOH溶液反应,发生转移的电子数为NA | |
| D. | 在20℃、1.0×105Pa条件下,11.2L氢气所含原子数为NA |
13.在KCl、MgSO4、MgCl2形成的混合溶液中,c(K+)=0.1mol/L,c(Mg2+)=0.25mol/L,c(Cl-)=0.2mol/L,则c(SO42-)为( )
| A. | 0.15 mol/L | B. | 0.20 mol/L | C. | 0.25 mol/L | D. | 0.40 mol/L |
10.下列有关方程式书写正确的是( )
| A. | NaHCO3的电离:NaHCO3?Na++H++CO32- | |
| B. | HS-的水解:HS-+H2O?H3O++S2- | |
| C. | 甲烷的标准燃烧热为-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O (g)△H=-890.3kJ•mol-1 | |
| D. | 双氧水中加入稀硫酸和KI溶液:H2O2+2I-+2H+═I2+2H2O |
17.有关性质或反应的离子方程式表示错误的是( )
| A. | 硫酸亚铁酸性溶液暴露在空气中:4Fe2++O2+4H+═4Fe3++2H2O | |
| B. | 过量石灰水与碳酸氢钙反应:Ca2++2HCO${\;}_{3}^{-}$+2OH-═CaCO3↓+CO${\;}_{3}^{2-}$+2H2O | |
| C. | 向偏铝酸钠溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO${\;}_{3}^{-}$ | |
| D. | 过量铁和稀硝酸反应:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O |
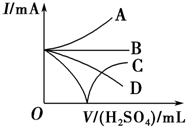 向Ba(OH)2溶液中加入稀硫酸,请完成下列问题:
向Ba(OH)2溶液中加入稀硫酸,请完成下列问题: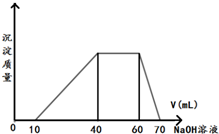 有一澄清透明的溶液,可能有NH4+、Fe3+、H+、Mg2+、Al3+、I-、CO32-等离子,现分别取溶液进行下列实验:
有一澄清透明的溶液,可能有NH4+、Fe3+、H+、Mg2+、Al3+、I-、CO32-等离子,现分别取溶液进行下列实验: